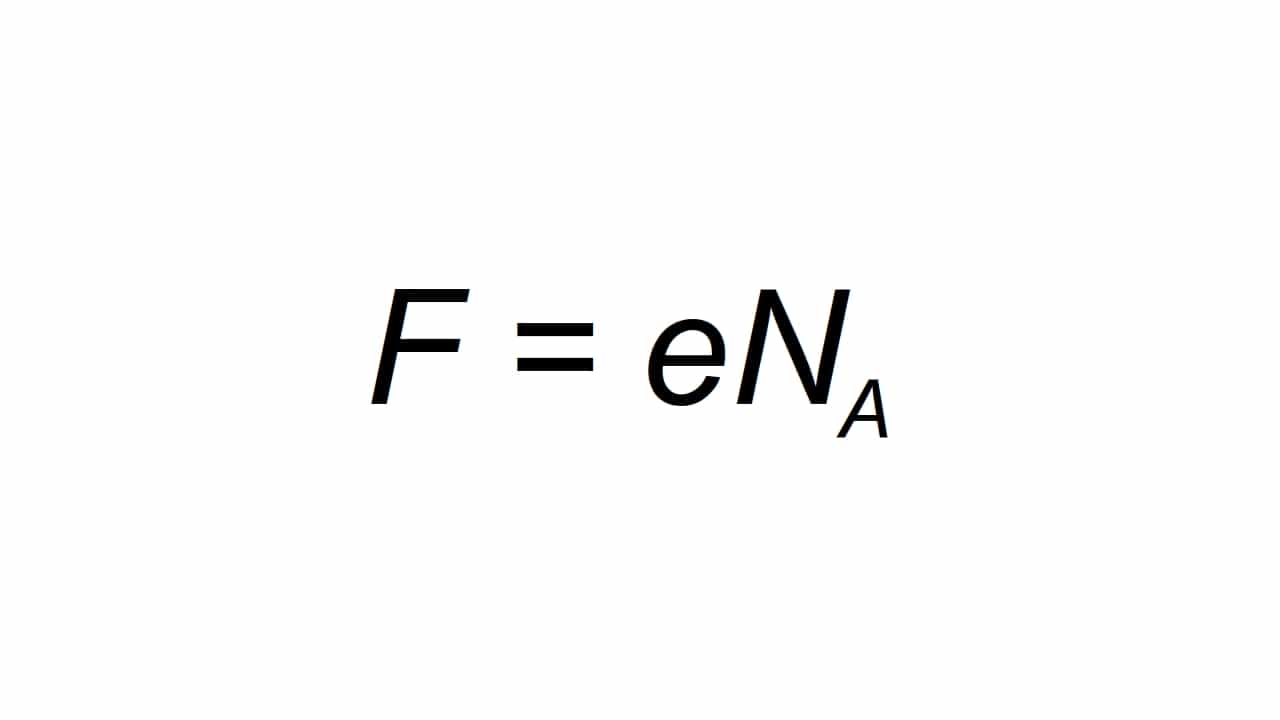Както и в други случаи, ние коментирахме други основни въпроси в областта на електрониката и електричеството, като например Законът на Ом, вълни Законите на Кирхофи дори видове основни електрически вериги, също би било интересно да се знае какво е това Фарадей е постоянен, тъй като може да ви помогне да знаете малко повече за натоварванията.
В тази статия ще разберете малко по -добре какво е постоянно блаженство, за какво може да се кандидатства и как се изчислява ...
Каква е константата на Фарадей?
La Фарадей е постоянен това е константа, широко използвана в областта на физиката и химията. Определя се като количеството електрически заряд на мол електрони. Името му идва от британския учен Майкъл Фарадей. Тази константа може да се използва в електрохимичните системи за изчисляване на масата на елементите, които се образуват в електрод.
Тя може да бъде представена с буквата F, и се определя като моларен елементарен заряд, който е в състояние изчисли като:
същество F получената стойност на константата на Фардей, е елементарният електрически заряд, а Na е константата на Авогадро:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 мол-1
Според SI тази константа на Фарадей е точна, подобно на други константи, и нейната точна стойност е: 96485,3321233100184 С / мол. Както можете да видите, той се изразява в единица C / mol, тоест кулони на мол. И за да разберете какви са тези единици, ако все още не знаете, можете да продължите да четете следващите два раздела ...
Какво е бенка?
Un мол е единица, която измерва количеството на веществото. В рамките на SI на единици тя е една от 7 -те фундаментални величини. Във всяко вещество, било то елемент или химично съединение, има редица елементарни единици, които го съставят. Един мол би бил еквивалентен на 6,022 140 76 × 1023 елементарни обекти, което е фиксираната числова стойност на константата на Авогадро.
Тези елементарни единици могат да бъдат атом, молекула, йон, електрон, фотони или друг вид елементарни частици. Например, с това можете изчислете броя на атомите какво има в грам от дадено вещество.
В химия, бенката е фундаментална, тъй като позволява да се правят много изчисления за съставите, химичните реакции и т.н. Например за вода (H2О), имате реакция 2 H2 + О2 → 2 Н2O, тоест, че два мола водород (H2) и един мол кислород (O2) реагират, образувайки два мола вода. Освен това те могат да се използват и за изразяване на концентрация (виж моларността).
Какъв е електрическият заряд?
От друга страна, от електрически заряд Вече сме говорили в други случаи, това е присъщо физическо свойство на някои субатомни частици, които проявяват привличащи и отблъскващи сили между тях поради електромагнитни полета. Електромагнитното взаимодействие между заряда и електрическото поле е едно от четирите основни взаимодействия във физиката, заедно със силната ядрена сила, слабата ядрена сила и гравитационната сила.
За да се измери този електрически заряд, Кулон (С) или Кулон, и се определя като количеството заряд, пренасяно за една секунда от електрически ток с интензитет един ампер.
Приложения на константата на Фарадей

Ако се чудите какво практическо приложение Можете да имате тази константа на Фарадей, истината е, че имате доста, някои примери са:
- Поцинковане / анодиране: за процеси в металургичната промишленост, при които един метал се покрива с друг чрез електролиза. Например, когато стоманата е поцинкована със слой цинк, за да й придаде по -голяма устойчивост на корозия. В тези процеси металът, който трябва да бъде покрит, се използва като анод, а електролитът е разтворима сол на анодния материал.
- Пречистване на метали: може да се приложи и към формулите, използвани за пречистване на метали като мед, цинк, калай и др. Също и чрез процедури за електролиза.
- Химическо производство: за получаване на химични съединения тази константа също обикновено се използва.
- Химичен анализ: чрез електролиза може да се определи и химическият състав.
- Производство на газ: газове като кислород или водород, получени от вода чрез електролиза, също използват тази константа за изчисления.
- Медицина и естетикаЕлектролизата може да се използва и за стимулиране на определени нерви или лечение на определени проблеми, в допълнение към премахването на нежеланото окосмяване. Без константата не биха могли да бъдат разработени множество инструменти от този тип.
- Печат: За принтерите, процесите на електролиза се използват и за определени елементи.
- Електролитични кондензатори: добре познат електронен компонент, състоящ се от тънък слой от алуминиев оксид и алуминиев анод между електродите. Електролитът е смес от борна киселина, глицерин и амониев хидроксид. И по този начин се постигат тези големи възможности ...
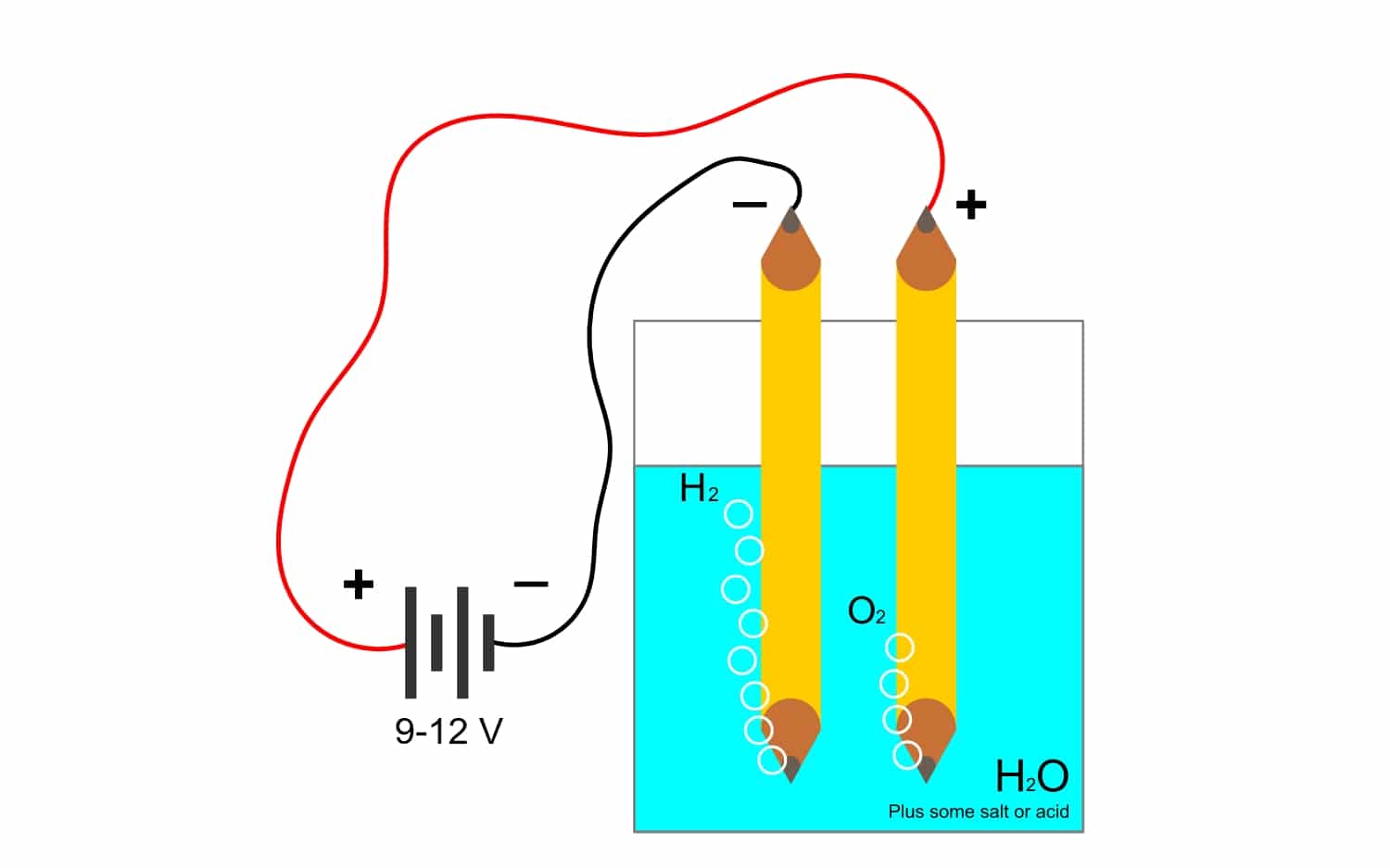
Какво е електролиза?
И тъй като константата на Фарадей е толкова тясно свързана с електролизаНека да видим какъв е този друг термин, който се използва много в индустрията. Благодарение на този процес елементите на съединението могат да бъдат разделени с помощта на електричество. Това става чрез освобождаване на електрони от анодните аниони (окисление) и улавяне на електрони от катодните катиони (редукция).
Той е открит случайно от Уилям Никълсън през 1800 г., докато изучава работата на химическите батерии. През 1834 г. Майкъл Фарадей разработи и публикува законите на електролизата.
Например, електролизата на вода Н2O, позволява създаването на кислород и водород. Ако се приложи постоянен ток през електроди, които ще отделят кислорода от водорода и ще могат да изолират двата газа (те не могат да влязат в контакт, тъй като те предизвикват много опасна експлозивна реакция).