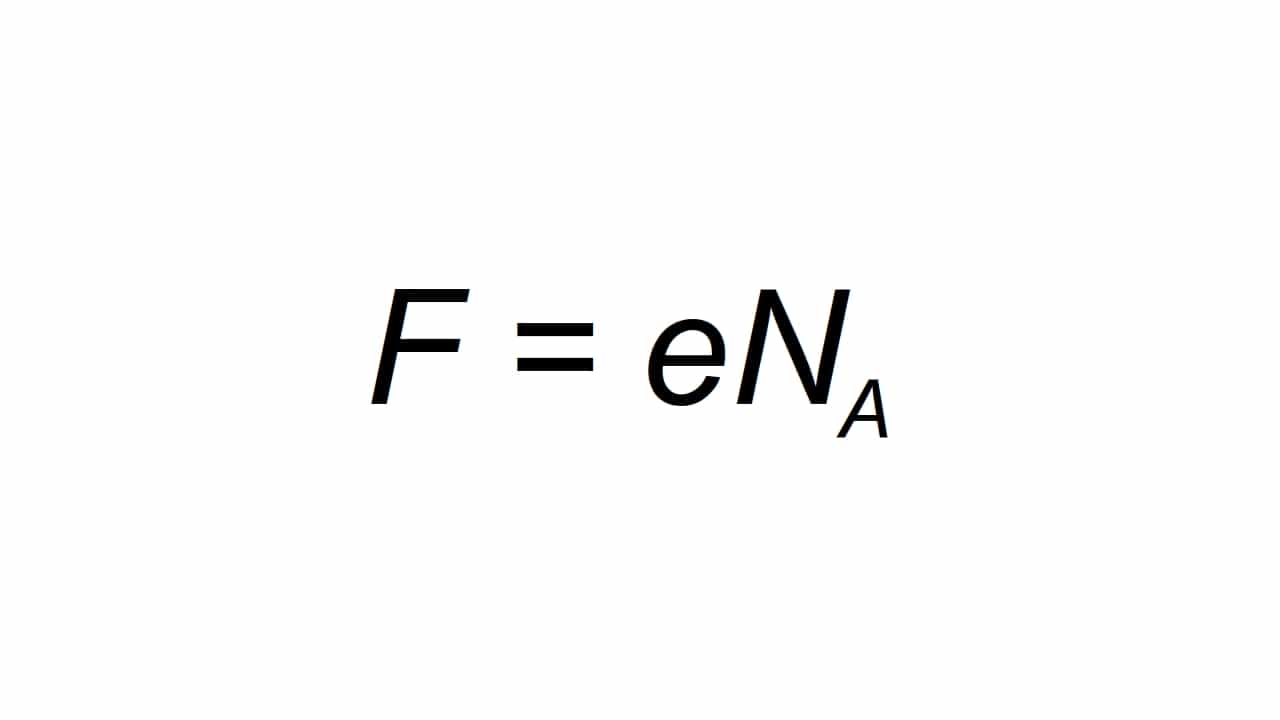Kao i drugi put, komentirali smo druga temeljna pitanja u području elektronike i električne energije, poput Ohmov zakon, valovi Kirchoffovi zakoni, pa čak i vrste osnovnih električnih kola, također bi bilo zanimljivo znati o čemu se radi Faraday je konstanta, jer vam može pomoći da saznate nešto više o opterećenjima.
U ovom ćete članku moći bolje razumjeti šta je stalno blaženstvo, za šta se sve to može prijaviti i kako se izračunava ...
Šta je Faradayeva konstanta?
La Faraday je konstanta to je konstanta koja se široko koristi u poljima fizike i hemije. Definira se kao količina električnog naboja po molu elektrona. Njegovo ime dolazi od britanskog naučnika Michaela Faradaya. Ova konstanta se može koristiti u elektrokemijskim sistemima za izračunavanje mase elemenata koji nastaju u elektrodi.
Može se predstaviti slovom F, i definira se kao molarni elementarni naboj, koji je sposoban calculate kao što su:
Biti F rezultirajuća vrijednost Fardayeve konstante, e elementarnog električnog naboja, a Na je Avogadrova konstanta:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 krtica-1
Prema SI ova Faradayeva konstanta je egzaktna, kao i ostale konstante, a njena precizna vrijednost je: 96485,3321233100184 C / mol. Kao što vidite, izražen je u jedinici C / mol, odnosno kulonima po molu. A da biste razumjeli koje su to jedinice, ako još ne znate, možete nastaviti čitati sljedeća dva odjeljka ...
Šta je madež?
Un krtica je jedinica koja mjeri količinu tvari. Unutar SI jedinica to je jedna od 7 osnovnih veličina. U bilo kojoj tvari, bilo da se radi o elementu ili kemijskom spoju, postoji niz elementarnih jedinica koje je čine. Jedan mol bio bi ekvivalentan 6,022 140 76 × 1023 elementarnih entiteta, što je fiksna numerička vrijednost Avogadrove konstante.
Ovi elementarni entiteti mogu biti atom, molekula, ion, elektron, fotoni ili bilo koja druga vrsta elementarne čestice. Na primjer, sa ovim možete izračunati broj atoma ono što se nalazi u gramu date supstance.
u hemija, krtica je fundamentalna, jer dopušta mnoge proračune za sastave, kemijske reakcije itd. Na primjer, za vodu (H2O), imate reakciju 2 H2 + ILI2 → 2H2O, odnosno dva mola vodika (H2) i jedan mol kisika (O2) reagiraju u dva mola vode. Nadalje, mogu se koristiti i za izražavanje koncentracije (vidi molarnost).
Šta je električni naboj?
S druge strane, iz električni naboj Već smo govorili u drugim prilikama, to je suštinsko fizičko svojstvo nekih subatomskih čestica koje ispoljavaju privlačne i odbojne sile među njima zbog elektromagnetskih polja. Elektromagnetska interakcija, između naboja i električnog polja, jedna je od 4 osnovne interakcije u fizici, zajedno s jakom nuklearnom silom, slabom nuklearnom silom i gravitacionom silom.
Za mjerenje ovog električnog naboja, Coulomb (C) ili Coulomb, i definira se kao količina naboja koju u jednoj sekundi nosi električna struja jačine jedan amper.
Primene Faradejeve konstante

Ako se pitate što praktična primjena Možete imati ovu Faradayevu konstantu, istina je da ih imate dosta, neki primjeri su:
- Galvanizacija / eloksiranje: za procese u metalurškoj industriji gdje je jedan metal prekriven drugim elektrolizom. Na primjer, kada je čelik pocinčan slojem cinka kako bi mu se dala veća otpornost na koroziju. U tim se postupcima metal koji se premazuje koristi kao anoda, a elektrolit je topljiva sol materijala anode.
- Pročišćavanje metala: može se primijeniti i na formule koje se koriste za oplemenjivanje metala poput bakra, cinka, kositra itd. Također postupcima elektrolize.
- Hemijska proizvodnja: za proizvodnju kemijskih spojeva ova se konstanta također obično koristi.
- Hemijska analiza: elektrolizom se može odrediti i hemijski sastav.
- Proizvodnja plina: plinovi poput kisika ili vodika koji se dobivaju iz vode elektrolizom također koriste ovu konstantu za proračune.
- Medicina i estetikaElektroliza se također može koristiti za stimulaciju određenih živaca ili liječenje određenih problema, osim uklanjanja neželjenih dlaka. Bez konstante ne bi se moglo razviti mnoštvo alata ove vrste.
- Usluge štampanja: Za štampače se procesi elektrolize koriste i za određene elemente.
- Elektrolitički kondenzatori: dobro poznata elektronička komponenta koja se sastoji od tankog filma aluminijevog oksida i aluminijske anode između elektroda. Elektrolit je mješavina borne kiseline, glicerina i amonijevog hidroksida. I ovako se postižu ti veliki kapaciteti ...
Šta je elektroliza?
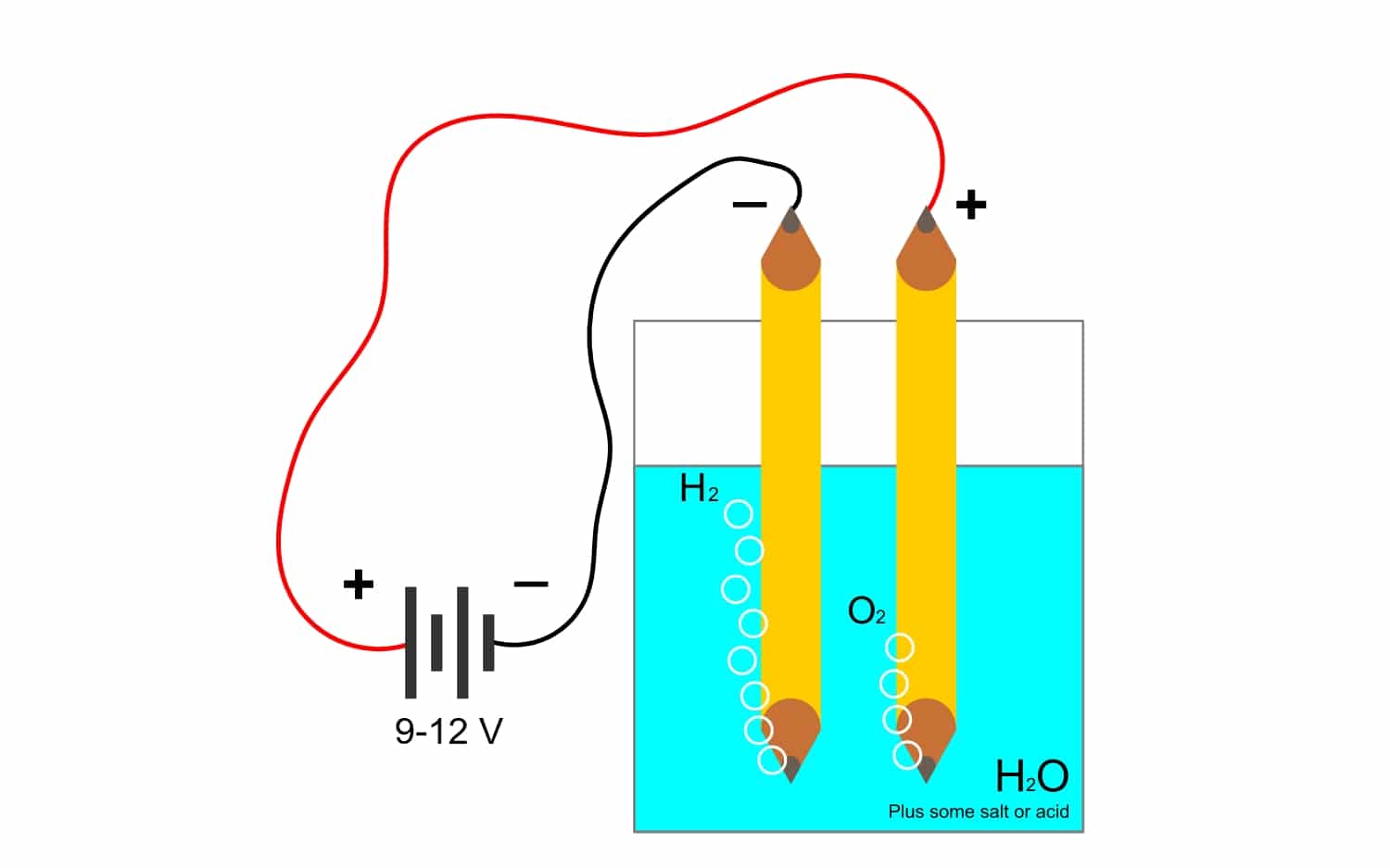
A budući da je Faradayeva konstanta toliko usko povezana sa elektrolizaPogledajmo koji je to drugi izraz koji se često koristi u industriji. Zahvaljujući ovom postupku, elementi spoja mogu se odvojiti pomoću električne energije. To se postiže oslobađanjem elektrona anodnim anionima (oksidacija) i hvatanjem elektrona katodnim kationima (redukcija).
Slučajno ga je otkrio William Nicholson 1800. godine, proučavajući rad hemijskih baterija. 1834. godine Michael Faraday razvio i objavio zakone elektrolize.
Na primjer, elektrolizom voda H2O, omogućuje stvaranje kisika i vodika. Ako se kroz elektrode primjenjuje istosmjerna struja koja će odvojiti kisik od vodika i moći će izolirati oba plina (oni ne mogu doći u kontakt jer proizvode vrlo opasnu eksplozivnu reakciju).