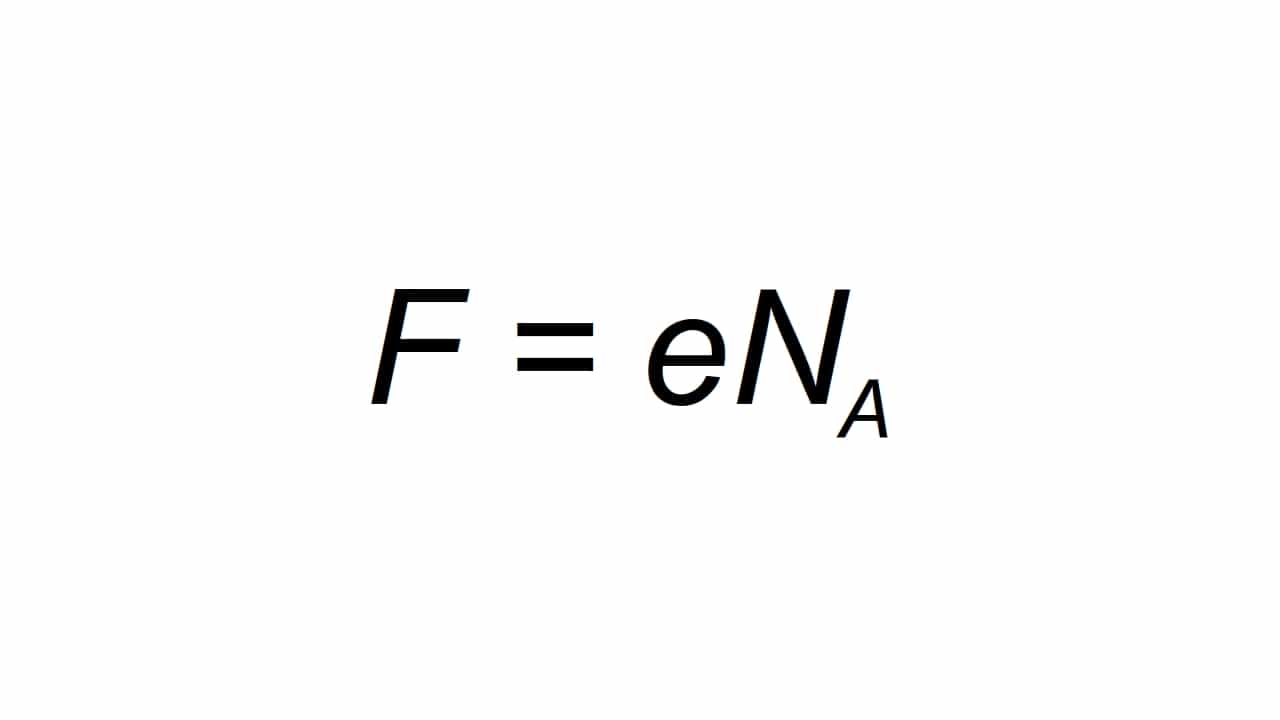A l'igual que altres vegades hem comentat sobre altres qüestions fonamentals en el camp de l'electrònica i l'electricitat, com la llei d'Ohm, O les lleis de Kirchoff, I fins i tot els tipus de circuits elèctrics bàsics, També seria interessant conèixer què és la constant de Faraday, Ja que et pot ajudar a saber una mica més de les càrregues.
En aquest article podràs comprendre una mica millor què és aquesta constant, Per a què es pot aplicar, i com es calcula ...
Què és la constant de Faraday?
La constant de Faraday és una constant molt emprada en els camps de la física i la química. Es defineix com la quantitat de càrrega elèctrica per mol d'electrons. El seu nom prové en honor a el científic britànic Michael Faraday. Aquesta constant es pot fer servir en els sistemes electroquímics per calcular la massa dels elements que es formen en un elèctrode.
Es pot representar per la lletra F, I es defineix com la càrrega elemental molar, podent-se Calcular com:
Sent F el valor resultant de la constant de Farday, i la càrrega elèctrica elemental, i Na la constant d'Avogadro:
- i = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mole-1
Segons el SI aquesta constant de Faraday és exacta, a l'igual que altres constants, i el seu valor precís és de: 96485,3321233100184 C / mol. Com pots veure, s'expressa en la unitat C / mol, és a dir, coulombs per mol. I per entendre què són aquestes unitats, si no ho saps encara, pots seguir llegint els dos següents apartats ...
Què és un mol?
Un mole és una unitat que mesura la quantitat de substància. Dins el SI d'unitats, és una de les 7 magnituds fonamentals. En qualsevol substància, ja sigui un element o un compost químic, hi ha una sèrie d'unitats elementals que el componen. Un mol seria equivalent a 6,022 140 76 × 1023 entitats elementals, que és el valor numèric fix de la constant d'Avogadro.
Aquestes entitats elementals poden ser un àtom, una molècula, un ió, un electró, fotons, o qualsevol altre tipus de partícula elemental. Per exemple, amb això es poden calcular la quantitat d'àtoms que hi ha en un gram d'una substància donada.
En la química, El mol és fonamental, ja que permet fer molts càlculs per a les composicions, reaccions químiques, etc. Per exemple, per a l'aigua (H2O), es té una reacció 2 H2 +O2 → 2 hores2O, És a dir, que dos mols d'hidrogen (H2) I un mol d'oxigen (O2) Reaccionen per formar dues mols d'aigua. A més, també es poden usar per a expressar la concentració (vegeu molaritat).
Què és la càrrega elèctrica?
D'altra banda, de la càrrega elèctrica ja hem parlat en altres ocasions, es tracta d'una propietat física intrínseca d'algunes partícules subatòmiques que manifesten forces d'atracció i repulsió entre elles a causa d'uns camps electromagnètics. La interacció electromagnètica, entre la càrrega i el camp elèctric, és una de les 4 interaccions fonamentals de la física, juntament amb la força nuclear forta, força nuclear feble, i la gravitatòria.
Per mesurar aquesta càrrega elèctrica s'empra el Coulomb (C) o Coulomb, I està definida com la quantitat de càrrega transportada en un segon per un corrent elèctric d'un ampere d'intensitat.
Aplicacions de la constant de Faraday

Si et preguntes què aplicació pràctica pot tenir aquesta constant de Faraday, la veritat és que té bastants, alguns exemples són:
- Galvanoplàstia / anodització: Per als processos de la indústria metal·lúrgica on un metall es recobreix d'un altre mitjançant electròlisi. Per exemple, quan l'acer es galvanitza amb una capa de zinc per donar-li major resistència a la corrosió. En aquests processos s'empra el metall a recobrir com a ànode i l'electròlit és una sal soluble de l'material de l'ànode.
- Purificació de metalls: També es pot aplicar a les fórmules emprades per al refinament de metalls com el coure, zinc, estany, etc. També per procediments d'electròlisi.
- Fabricació de químics: Per a produir compostos químics també se sol emprar aquesta constant.
- anàlisi química: Mitjançant electròlisi també es podria determinar la composició química.
- Producció de gasos: Gasos com l'oxigen o l'hidrogen que s'obtenen a partir d'l'aigua mitjançant electròlisi també fan servir aquesta constant per als càlculs.
- Medicina i estètica: També es poden usar electròlisi per estimular certs nervis o tractar certs problemes, a més d'eliminar el borrissol no desitjat. Sense la constant, no es podrien haver desenvolupat multitud d'eines d'aquest tipus.
- Impressió: Per a les impremtes també s'empren processos d'electròlisi per a certs elements.
- condensadors electrolítics: Un component electrònic molt conegut i que es compon d'una pel·lícula prima d'òxid d'alumini i un ànode d'alumini entre elèctrodes. L'electròlit és una barreja d'àcid bòric, gilcerina i hidròxid d'amoni. I així és com s'aconsegueixen aquestes capacitats tan grans ...
Què és l'electròlisi?
I ja que la constant de Faraday està tan relacionada amb la electròlisi, Anem a veure què és aquest altre terme que s'empra bastant en la indústria. Gràcies a aquest procés es poden separar elements d'un compost per mitjà d'electricitat. Això es fa mitjançant l'alliberament d'electrons pels anions de l'ànode (oxidació) i la captura d'electrons pels cations de el càtode (reducció).
Va ser descoberta accidentalment per William Nicholson, en 1800, mientrs estudiava el funcionament de les bateries químiques. En 1834, Michael Faraday va desenvolupar i va publicar les lleis de l'electròlisi.
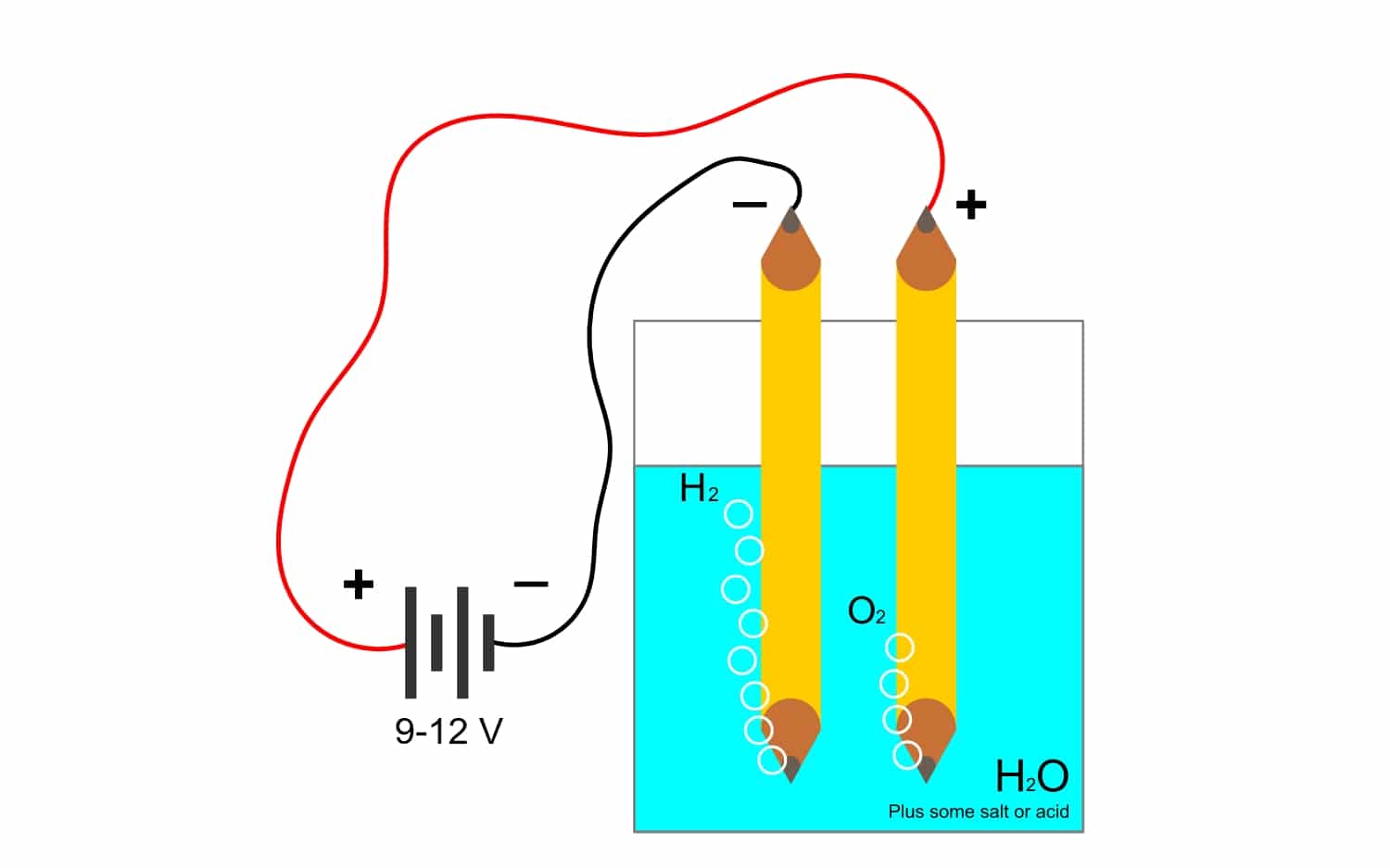
Per exemple, l'electròlisi de l' aigua H2O, Permet crear oxigen i hidrogen. Si se li aplica un corrent continu a través d'uns elèctrodes, el que aconseguirà separar l'oxigen de l'hidrogen, i poder aïllar els dos gasos (no poden entrar en contacte, ja que produeixen una reacció explosiva molt perillosa).