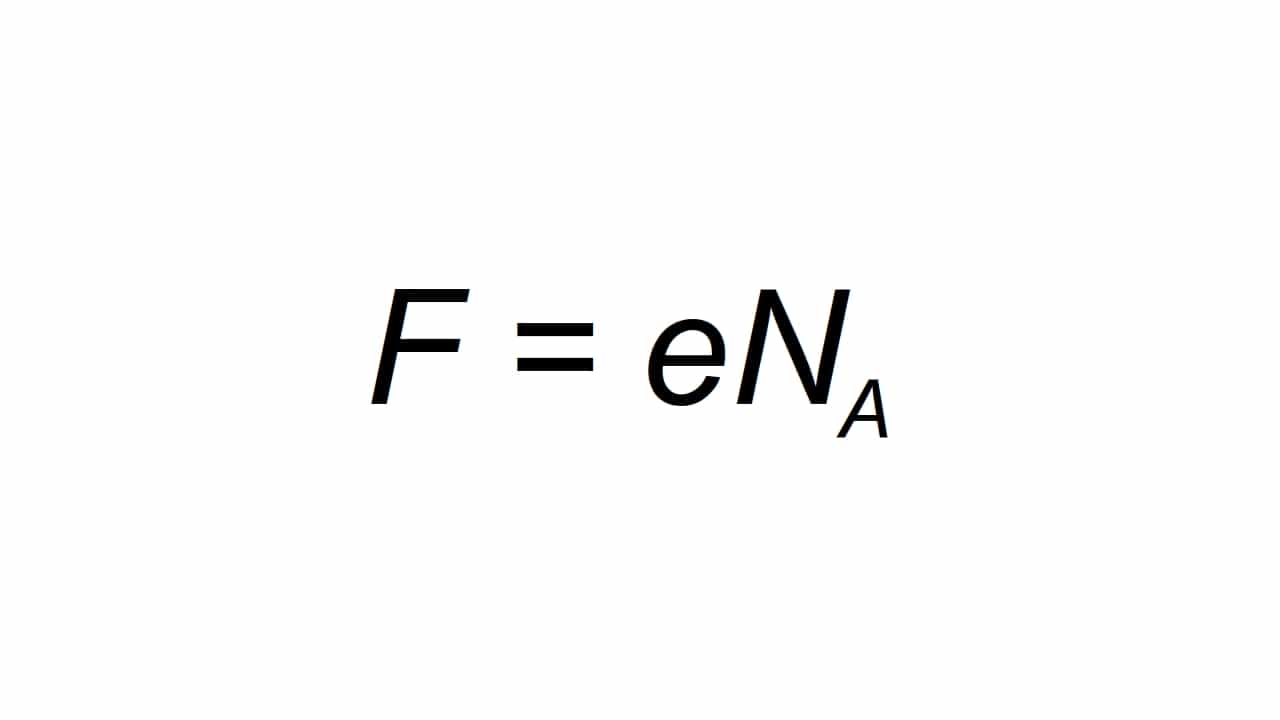Stejně jako jindy jsme se vyjádřili k dalším zásadním otázkám v oblasti elektroniky a elektřiny, jako např Ohmův zákon, vlny Kirchoffovy zákony, a dokonce i typy základních elektrických obvodů„Bylo by také zajímavé vědět, co to je Faradayova konstanta, protože vám může pomoci dozvědět se trochu více o nákladech.
V tomto článku budete moci trochu lépe porozumět co je neustálá blaženostO co lze žádat a jak se vypočítává ...
Co je Faradayova konstanta?
La Faradayova konstanta je to konstanta široce používaná v oblasti fyziky a chemie. Je definována jako množství elektrického náboje na mol elektronů. Její název pochází od britského vědce Michaela Faradaye. Tuto konstantu lze použít v elektrochemických systémech k výpočtu hmotnosti prvků, které se tvoří v elektrodě.
Může být reprezentován písmenem F, a je definován jako molární elementární náboj, schopný vypočítat jako:
Být F výsledná hodnota Fardayovy konstanty, e elementárního elektrického náboje, a Na je Avogadrova konstanta:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Podle SI je tato Faradayova konstanta přesná, stejně jako ostatní konstanty, a její přesná hodnota je: 96485,3321233100184 C / mol. Jak vidíte, vyjadřuje se v jednotce C / mol, tj. Coulombů na mol. A abyste pochopili, co tyto jednotky jsou, pokud ještě nevíte, můžete pokračovat ve čtení dalších dvou částí ...
Co je krtek?
Un mol je jednotka, která měří množství látky. V rámci SI jednotek je to jedna ze 7 základních veličin. V každé látce, ať už je to prvek nebo chemická sloučenina, existuje řada elementárních jednotek, které ji tvoří. Jeden mol by odpovídal 6,022 140 76 × 1023 elementárních entit, což je pevná číselná hodnota Avogadrovy konstanty.
Těmito elementárními entitami mohou být atom, molekula, iont, elektron, fotony nebo jakýkoli jiný typ elementárních částic. Například s tímto můžete vypočítat počet atomů co je v gramu dané látky.
V chemie„mol je zásadní, protože umožňuje provádět mnoho výpočtů pro složení, chemické reakce atd. Například pro vodu (H.2O), máte reakci 2 H2 + O.2 → 2H2O, to znamená, že dva moly vodíku (H.2) a jeden mol kyslíku (O2) reagují za vzniku dvou molů vody. Kromě toho mohou být také použity k vyjádření koncentrace (viz molarita).
Co je to elektrický náboj?
Na druhou stranu z elektrický náboj Už jsme hovořili při jiných příležitostech, je to vnitřní fyzikální vlastnost některých subatomárních částic, které mezi nimi v důsledku elektromagnetických polí projevují přitažlivé a odpudivé síly. Elektromagnetická interakce mezi nábojem a elektrickým polem je jednou ze 4 základních interakcí ve fyzice spolu se silnou jadernou silou, slabou jadernou silou a gravitační silou.
K měření tohoto elektrického náboje Coulomb (C) nebo Coulomb, a je definován jako množství náboje přeneseného za jednu sekundu elektrickým proudem o intenzitě jeden ampér.
Aplikace Faradayovy konstanty

Pokud vás zajímá, co praktická aplikace Můžete mít tuto Faradayovu konstantu, pravdou je, že jich máte docela dost, některé příklady jsou:
- Galvanické pokovování / eloxování: pro procesy v hutním průmyslu, kde je jeden kov elektrolýzou potažen druhým. Například když je ocel pozinkována vrstvou zinku, aby získala větší odolnost proti korozi. V těchto procesech se kov, který má být potahován, používá jako anoda a elektrolyt je rozpustná sůl anodového materiálu.
- Čištění kovů: lze jej také použít na vzorce používané pro zušlechťování kovů, jako je měď, zinek, cín atd. Také postupy elektrolýzy.
- Chemická výroba: k výrobě chemických sloučenin se tato konstanta také obvykle používá.
- Chemický rozbor: elektrolýzou lze také určit chemické složení.
- Výroba plynu: tuto konstantu pro výpočty používají také plyny jako kyslík nebo vodík, které se získávají z vody elektrolýzou.
- Lékařství a estetikaElektrolýzu lze kromě odstranění nežádoucích chloupků použít také ke stimulaci určitých nervů nebo léčbě určitých problémů. Bez konstanty by nebylo možné vyvinout mnoho nástrojů tohoto typu.
- Vytisknout: U tiskáren se pro určité prvky používají také procesy elektrolýzy.
- Elektrolytické kondenzátory: známá elektronická součást sestávající z tenkého filmu oxidu hlinitého a hliníkové anody mezi elektrodami. Elektrolyt je směs kyseliny borité, glycerinu a hydroxidu amonného. A takto se dosahuje těch skvělých kapacit ...
Co je elektrolýza?
A protože Faradayova konstanta tak úzce souvisí s elektrolýzaPodívejme se, jaký je tento další termín, který se v průmyslu hodně používá. Díky tomuto procesu lze prvky sloučeniny oddělit pomocí elektřiny. To se provádí uvolněním elektronů anodovými anionty (oxidace) a zachycením elektronů katodovými kationty (redukce).
Objevil jej náhodně William Nicholson v roce 1800 při studiu provozu chemických baterií. V roce 1834, Michael Faraday vyvinul a publikoval zákony elektrolýzy.
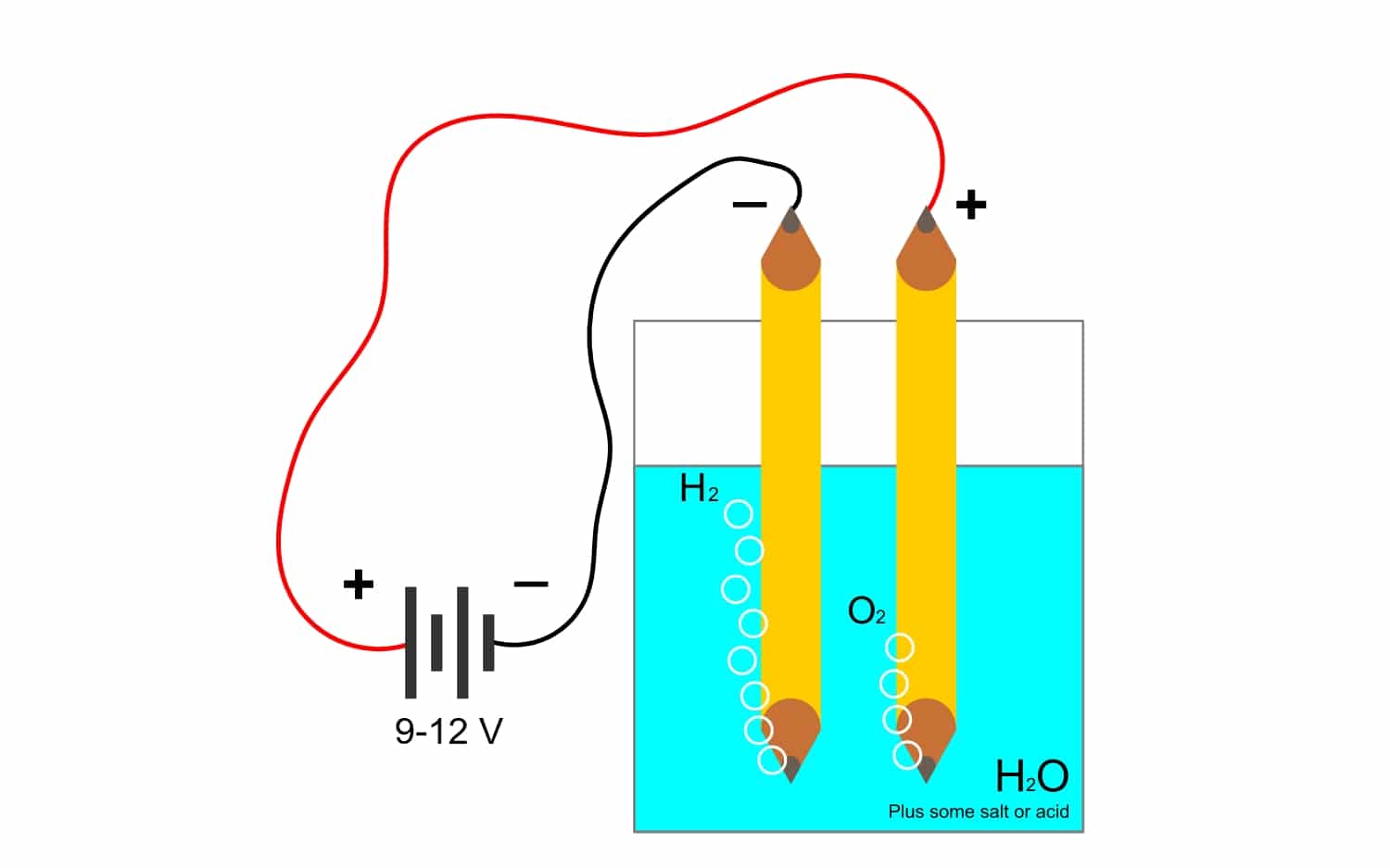
Například elektrolýza voda H.2O, umožňuje vytvářet kyslík a vodík. Pokud je na elektrody přiváděn stejnosměrný proud, který odděluje kyslík od vodíku a je schopen izolovat oba plyny (nemohou přijít do styku, protože vyvolávají velmi nebezpečnou výbušnou reakci).