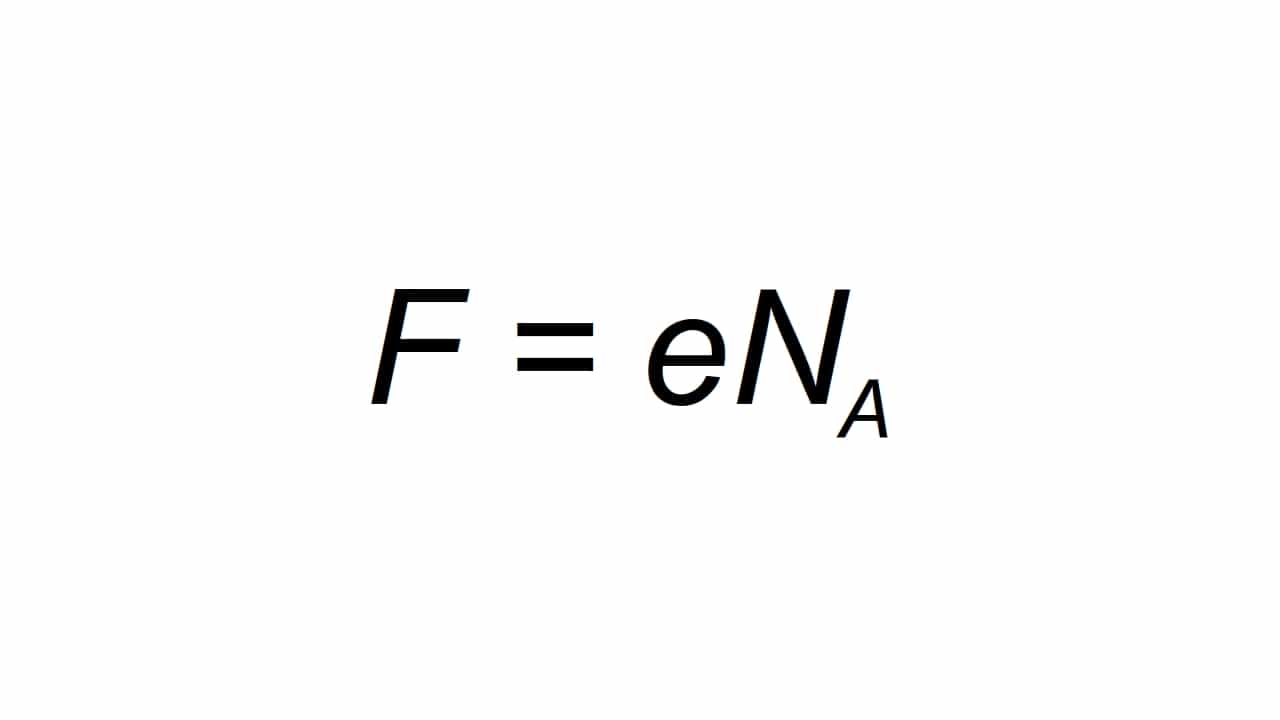Wie zu anderen Zeiten haben wir uns zu anderen grundlegenden Fragen im Bereich der Elektronik und Elektrizität geäußert, wie z Ohm'sches Gesetz, O las Kirchoffsche Gesetzeund sogar die Arten von elektrischen Grundschaltungen, es wäre auch interessant zu wissen, was es ist Faradays Konstante, da es Ihnen helfen kann, ein wenig mehr über die Lasten zu erfahren.
In diesem Artikel werden Sie es etwas besser verstehen Was ist ständige Glückseligkeit?, wofür kann es beantragt werden und wie wird es berechnet ...
Was ist die Faraday-Konstante?
La Faradays Konstante es ist eine Konstante, die in den Bereichen Physik und Chemie weit verbreitet ist. Es ist definiert als die Menge an elektrischer Ladung pro Mol Elektronen. Sein Name stammt von dem britischen Wissenschaftler Michael Faraday. Diese Konstante kann in elektrochemischen Systemen verwendet werden, um die Masse der Elemente zu berechnen, die sich in einer Elektrode bilden.
Es kann durch den Buchstaben dargestellt werden F, und ist definiert als die molare Elementarladung, die in der Lage ist Calcular als:
Sein F der resultierende Wert der Fardayschen Konstanten, e der elementaren elektrischen Ladung, und Na ist die Avogadro-Konstante:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Laut SI ist diese Faraday-Konstante genau wie andere Konstanten und ihr genauer Wert ist: 96485,3321233100184 C / mol. Wie Sie sehen können, wird es in der Einheit C / Mol ausgedrückt, dh Coulomb pro Mol. Und um zu verstehen, was diese Einheiten sind, können Sie, wenn Sie es noch nicht wissen, die nächsten beiden Abschnitte weiterlesen ...
Was ist ein Maulwurf?
Un mol ist eine Einheit, die die Stoffmenge misst. Innerhalb der SI-Einheiten ist sie eine der 7 fundamentalen Größen. In jeder Substanz, sei es ein Element oder eine chemische Verbindung, gibt es eine Reihe elementarer Einheiten, aus denen sie besteht. Ein Mol würde 6,022 140 76 × 10 . entsprechen23 elementare Entitäten, das ist der feste numerische Wert der Avogadro-Konstante.
Diese elementaren Einheiten können ein Atom, ein Molekül, ein Ion, ein Elektron, Photonen oder jede andere Art von Elementarteilchen sein. Damit kannst du zum Beispiel Berechnen Sie die Anzahl der Atome was ist in einem Gramm einer bestimmten Substanz.
Im Chemie, ist der Mol von grundlegender Bedeutung, da er viele Berechnungen für Zusammensetzungen, chemische Reaktionen usw. Zum Beispiel für Wasser (H2O), du hast eine Reaktion 2 H2 + O2 → 2 Std2O, d. h. zwei Mol Wasserstoff (H2) und ein Mol Sauerstoff (O2) reagieren zu zwei Mol Wasser. Darüber hinaus können sie auch verwendet werden, um die Konzentration auszudrücken (siehe Molarität).
Wie hoch ist die elektrische Ladung?
Auf der anderen Seite aus dem elektrische Ladung Wir haben bereits bei anderen Gelegenheiten gesprochen, es ist eine intrinsische physikalische Eigenschaft einiger subatomarer Teilchen, die aufgrund elektromagnetischer Felder anziehende und abstoßende Kräfte zwischen ihnen manifestieren. Die elektromagnetische Wechselwirkung zwischen Ladung und elektrischem Feld ist neben der starken Kernkraft, der schwachen Kernkraft und der Gravitationskraft eine der 4 fundamentalen Wechselwirkungen in der Physik.
Um diese elektrische Ladung zu messen, Coulomb (C) oder Coulomb, und ist definiert als die Ladungsmenge, die in einer Sekunde von einem elektrischen Strom mit einer Stärke von einem Ampere transportiert wird.
Anwendungen der Faraday-Konstanten

Wenn Sie sich fragen, was praktische Anwendung Sie können diese Faraday-Konstante haben, die Wahrheit ist, dass Sie einige haben, einige Beispiele sind:
- Galvanisieren / Eloxieren: für Prozesse in der metallurgischen Industrie, bei denen ein Metall durch Elektrolyse mit einem anderen überzogen wird. Zum Beispiel, wenn Stahl mit einer Zinkschicht galvanisiert wird, um ihm eine höhere Korrosionsbeständigkeit zu verleihen. Bei diesen Verfahren wird das zu beschichtende Metall als Anode verwendet und der Elektrolyt ist ein lösliches Salz des Anodenmaterials.
- Metallreinigung: kann auch auf die Formeln angewendet werden, die zur Veredelung von Metallen wie Kupfer, Zink, Zinn usw. verwendet werden. Auch durch Elektrolyseverfahren.
- Chemische Herstellung: Um chemische Verbindungen herzustellen, wird diese Konstante normalerweise auch verwendet.
- Chemische Analyse: Durch Elektrolyse konnte auch die chemische Zusammensetzung bestimmt werden.
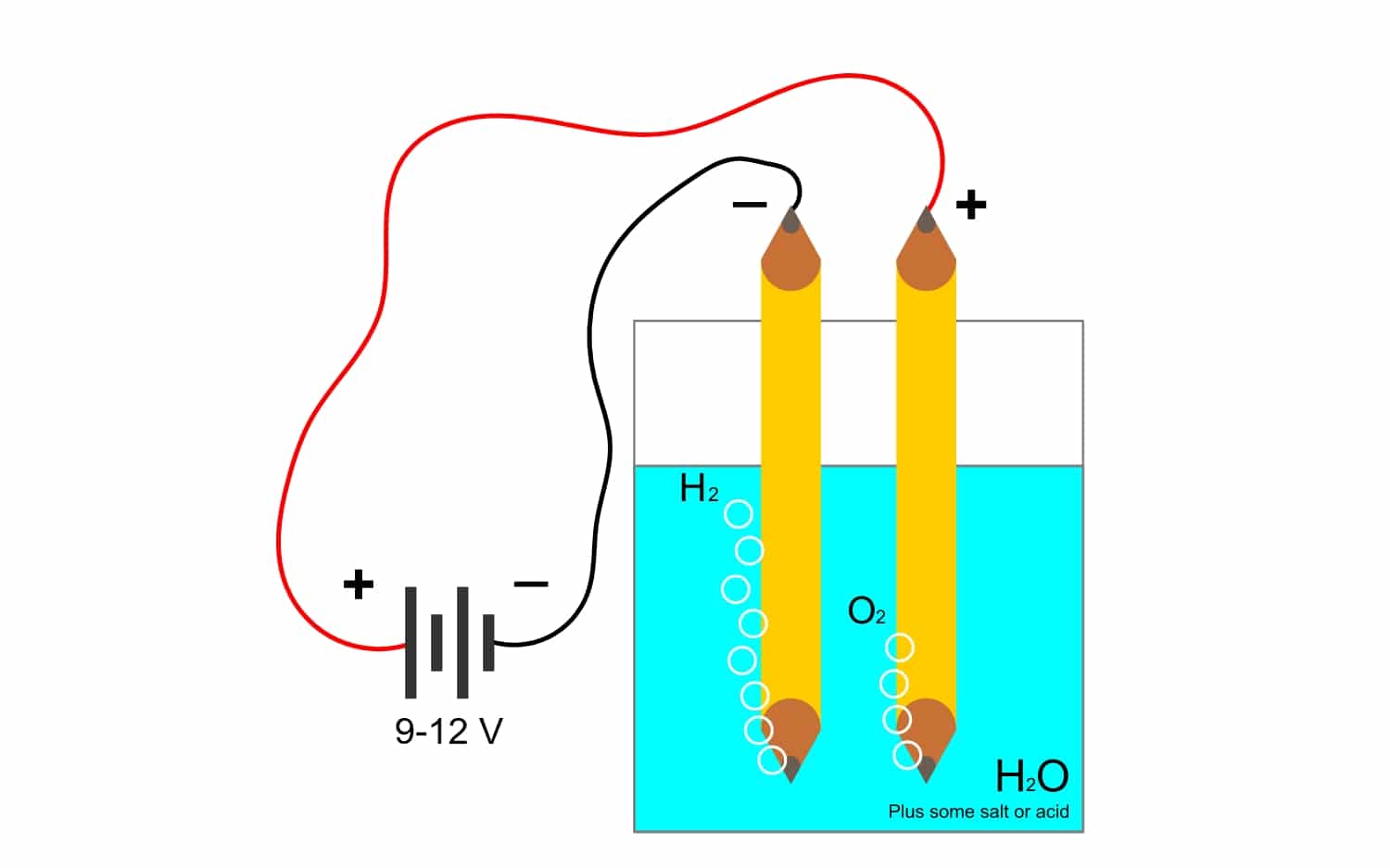
- Gasproduktion: Gase wie Sauerstoff oder Wasserstoff, die durch Elektrolyse aus Wasser gewonnen werden, verwenden diese Konstante ebenfalls für Berechnungen.
- Medizin und ÄsthetikDie Elektrolyse kann auch verwendet werden, um bestimmte Nerven zu stimulieren oder bestimmte Probleme zu behandeln, sowie unerwünschte Haare zu entfernen. Ohne die Konstante wäre eine Vielzahl von Werkzeugen dieser Art nicht zu entwickeln.
- Impresión: Bei Druckern werden für bestimmte Elemente auch Elektrolyseverfahren eingesetzt.
- Elektrolytkondensator: ein bekanntes elektronisches Bauteil, das aus einem dünnen Film aus Aluminiumoxid und einer Aluminiumanode zwischen den Elektroden besteht. Der Elektrolyt ist eine Mischung aus Borsäure, Glycerin und Ammoniumhydroxid. Und so werden diese großen Kapazitäten erreicht ...
Was ist Elektrolyse?
Und da die Faraday-Konstante so eng mit der ElektrolyseMal sehen, was dieser andere Begriff ist, der in der Branche häufig verwendet wird. Dank dieses Verfahrens können Elemente einer Verbindung mit Hilfe von Elektrizität getrennt werden. Dies geschieht durch die Abgabe von Elektronen durch die Anodenanionen (Oxidation) und den Einfang von Elektronen durch die Kathodenkationen (Reduktion).
Es wurde 1800 zufällig von William Nicholson entdeckt, als er die Funktionsweise chemischer Batterien untersuchte. Im Jahr 1834, Michael Faraday die Gesetze der Elektrolyse entwickelt und veröffentlicht.
Zum Beispiel die Elektrolyse von Wasser H2O, ermöglicht die Erzeugung von Sauerstoff und Wasserstoff. Wenn über Elektroden ein Gleichstrom angelegt wird, der den Sauerstoff vom Wasserstoff trennt und beide Gase isolieren kann (sie können nicht in Kontakt kommen, da sie eine sehr gefährliche explosive Reaktion erzeugen).