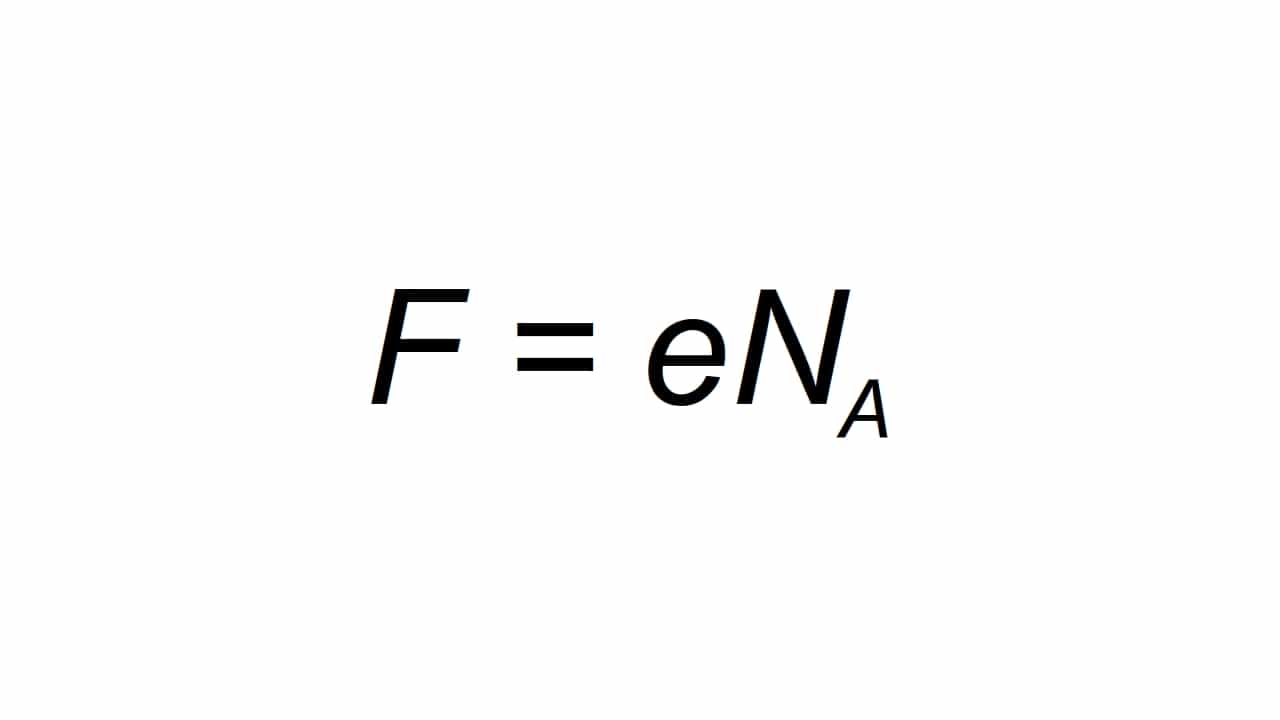Όπως και άλλες φορές έχουμε σχολιάσει άλλα θεμελιώδη ερωτήματα στον τομέα των ηλεκτρονικών και της ηλεκτρικής ενέργειας, όπως το Ο νόμος του Ωμ, κύματα Οι νόμοι του Κίρχοφ, ακόμη και το είδη βασικών ηλεκτρικών κυκλωμάτων, θα ήταν επίσης ενδιαφέρον να γνωρίζουμε τι είναι Η σταθερά του Φαραντέι, καθώς μπορεί να σας βοηθήσει να μάθετε λίγο περισσότερα για τα φορτία.
Σε αυτό το άρθρο θα καταλάβετε λίγο καλύτερα τι είναι σταθερή ευδαιμονία, για τι μπορεί να εφαρμοστεί και πώς υπολογίζεται ...
Τι είναι η σταθερά Faraday;
La Η σταθερά του Φαραντέι είναι μια σταθερά που χρησιμοποιείται ευρέως στους τομείς της φυσικής και της χημείας. Ορίζεται ως η ποσότητα ηλεκτρικού φορτίου ανά γραμμόνιο ηλεκτρονίων. Το όνομά του προέρχεται από τον Βρετανό επιστήμονα Michael Faraday. Αυτή η σταθερά μπορεί να χρησιμοποιηθεί σε ηλεκτροχημικά συστήματα για τον υπολογισμό της μάζας των στοιχείων που σχηματίζονται σε ένα ηλεκτρόδιο.
Μπορεί να αναπαρασταθεί με το γράμμα F, και ορίζεται ως το γραμμομοριακό στοιχειώδες φορτίο, είναι σε θέση για να υπολογίσετε όπως:
Όντας F την προκύπτουσα τιμή της σταθεράς του Farday, e το στοιχειώδες ηλεκτρικό φορτίο, και Na είναι η σταθερά του Avogadro:
- e = 1.602176634 10-19 C
- Na = 6.02214076 1023 mole-1
Σύμφωνα με το SI, αυτή η σταθερά Faraday είναι ακριβής, όπως και άλλες σταθερές, και η ακριβής τιμή της είναι: 96485,3321233100184 C / molΤο Όπως μπορείτε να δείτε, εκφράζεται στη μονάδα C / mol, δηλαδή, κουλόνια ανά γραμμομόριο. Και για να καταλάβετε τι είναι αυτές οι μονάδες, εάν δεν γνωρίζετε ακόμη, μπορείτε να συνεχίσετε να διαβάζετε τις επόμενες δύο ενότητες ...
Τι είναι ο τυφλοπόντικας;
Un mole είναι μια μονάδα που μετρά την ποσότητα της ουσίας. Μέσα στο SI των μονάδων, είναι ένα από τα 7 θεμελιώδη μεγέθη. Σε οποιαδήποτε ουσία, είτε πρόκειται για στοιχείο είτε για χημική ένωση, υπάρχει μια σειρά στοιχειωδών μονάδων που την συνθέτουν. Ένα mole θα ισοδυναμεί με 6,022 140 76 × 1023 στοιχειώδεις οντότητες, η οποία είναι η σταθερή αριθμητική τιμή της σταθεράς του Avogadro.
Αυτές οι στοιχειώδεις οντότητες μπορεί να είναι ένα άτομο, ένα μόριο, ένα ιόν, ένα ηλεκτρόνιο, φωτόνια ή οποιοσδήποτε άλλος τύπος στοιχειακού σωματιδίου. Για παράδειγμα, με αυτό μπορείτε υπολογίστε τον αριθμό των ατόμων τι υπάρχει σε ένα γραμμάριο μιας δεδομένης ουσίας.
Στην χημεία, ο τυφλοπόντικας είναι απαραίτητος, αφού επιτρέπει πολλούς υπολογισμούς για συνθέσεις, χημικές αντιδράσεις κ.λπ. Για παράδειγμα, για νερό (Η2Ο), έχετε αντίδραση Η 22 + Ο2 → 2 Ω2O, δηλαδή, ότι δύο γραμμομόρια υδρογόνου (Η2) και ένα γραμμομόριο οξυγόνου (Ο2) αντιδρούν σχηματίζοντας δύο moles νερού. Επιπλέον, μπορούν επίσης να χρησιμοποιηθούν για να εκφράσουν τη συγκέντρωση (βλέπε μοριακότητα).
Τι είναι το ηλεκτρικό φορτίο;
Από την άλλη πλευρά, από το ηλεκτρικό φορτίο Έχουμε ήδη μιλήσει σε άλλες περιπτώσεις, είναι μια εγγενής φυσική ιδιότητα ορισμένων υποατομικών σωματιδίων που εκδηλώνουν ελκυστικές και απωθητικές δυνάμεις μεταξύ τους λόγω ηλεκτρομαγνητικών πεδίων. Η ηλεκτρομαγνητική αλληλεπίδραση, μεταξύ φορτίου και ηλεκτρικού πεδίου, είναι μία από τις 4 θεμελιώδεις αλληλεπιδράσεις στη φυσική, μαζί με την ισχυρή πυρηνική δύναμη, την αδύναμη πυρηνική δύναμη και τη βαρυτική δύναμη.
Για να μετρήσετε αυτό το ηλεκτρικό φορτίο, το Coulomb (C) ή Coulomb, και ορίζεται ως η ποσότητα φορτίου που μεταφέρεται σε ένα δευτερόλεπτο από ηλεκτρικό ρεύμα έντασης ένα αμπέρ.
Εφαρμογές της σταθεράς Faraday

Αν αναρωτιέστε τι Πρακτική εφαρμογη Μπορείτε να έχετε αυτήν τη σταθερά Faraday, η αλήθεια είναι ότι έχετε αρκετά, μερικά παραδείγματα είναι:
- Επιμετάλλωση / ανοδίωση: για διαδικασίες στη μεταλλουργική βιομηχανία όπου ένα μέταλλο καλύπτεται με άλλο με ηλεκτρόλυση. Για παράδειγμα, όταν ο χάλυβας γαλβανίζεται με ένα στρώμα ψευδαργύρου για να του δώσει μεγαλύτερη αντοχή στη διάβρωση. Σε αυτές τις διαδικασίες, το μέταλλο που πρόκειται να επικαλυφθεί χρησιμοποιείται ως άνοδος και ο ηλεκτρολύτης είναι ένα διαλυτό άλας του υλικού της ανόδου.
- Καθαρισμός μετάλλων: μπορεί επίσης να εφαρμοστεί στους τύπους που χρησιμοποιούνται για τη βελτίωση μετάλλων όπως χαλκός, ψευδάργυρος, κασσίτερος κ.λπ. Επίσης με διαδικασίες ηλεκτρόλυσης.
- Χημική κατασκευή: για την παραγωγή χημικών ενώσεων αυτή η σταθερά χρησιμοποιείται επίσης συνήθως.
- Χημική ανάλυση: με ηλεκτρόλυση θα μπορούσε επίσης να προσδιοριστεί η χημική σύνθεση.
- Παραγωγή αερίου: αέρια όπως οξυγόνο ή υδρογόνο που λαμβάνονται από το νερό με ηλεκτρόλυση χρησιμοποιούν επίσης αυτή τη σταθερά για υπολογισμούς.
- Ιατρική και αισθητικήΗ ηλεκτρόλυση μπορεί επίσης να χρησιμοποιηθεί για την τόνωση ορισμένων νεύρων ή τη θεραπεία ορισμένων προβλημάτων, εκτός από την αφαίρεση των ανεπιθύμητων τριχών. Χωρίς τη σταθερά, ένα πλήθος εργαλείων αυτού του τύπου δεν θα μπορούσε να έχει αναπτυχθεί.
- Εκτύπωση: Για εκτυπωτές, οι διαδικασίες ηλεκτρόλυσης χρησιμοποιούνται επίσης για ορισμένα στοιχεία.
- Ηλεκτρολυτικοί πυκνωτές: ένα πολύ γνωστό ηλεκτρονικό συστατικό που αποτελείται από μια λεπτή μεμβράνη οξειδίου του αργιλίου και μια άνοδο αλουμινίου μεταξύ ηλεκτροδίων. Ο ηλεκτρολύτης είναι ένα μείγμα βορικού οξέος, γλυκερίνης και υδροξειδίου του αμμωνίου. Και κάπως έτσι επιτυγχάνονται αυτές οι μεγάλες ικανότητες ...
Τι είναι η ηλεκτρόλυση;
Και δεδομένου ότι η σταθερά Faraday σχετίζεται τόσο στενά με το ηλεκτρόλυσηΑς δούμε τι είναι αυτός ο άλλος όρος που χρησιμοποιείται πολύ στη βιομηχανία. Χάρη σε αυτή τη διαδικασία, τα στοιχεία μιας ένωσης μπορούν να διαχωριστούν μέσω ηλεκτρικής ενέργειας. Αυτό γίνεται με την απελευθέρωση ηλεκτρονίων από τα ανιόντα ανόδου (οξείδωση) και τη δέσμευση των ηλεκτρονίων από τα κατιόντα καθόδου (αναγωγή).
Ανακαλύφθηκε τυχαία από τον William Nicholson, το 1800, ενώ μελετούσε τη λειτουργία των χημικών μπαταριών. Το 1834, Μιχάλης Φαραντέι ανέπτυξε και δημοσίευσε τους νόμους της ηλεκτρόλυσης.
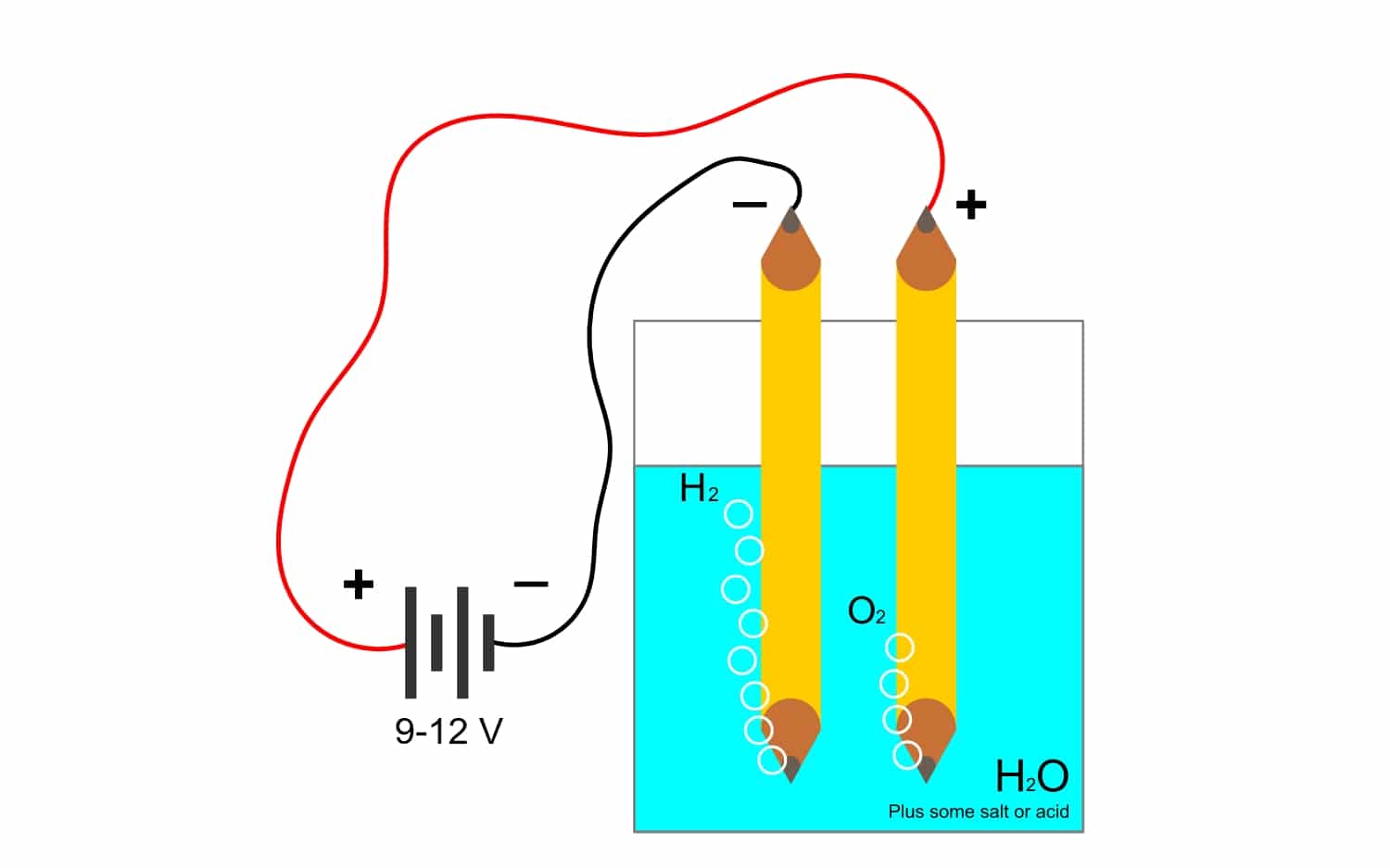
Για παράδειγμα, η ηλεκτρόλυση του νερό Η2O, επιτρέπει τη δημιουργία οξυγόνου και υδρογόνου. Εάν εφαρμοστεί ένα συνεχές ρεύμα μέσω ηλεκτροδίων, το οποίο θα διαχωρίσει το οξυγόνο από το υδρογόνο και θα είναι σε θέση να απομονώσει και τα δύο αέρια (δεν μπορούν να έρθουν σε επαφή, καθώς προκαλούν μια πολύ επικίνδυνη εκρηκτική αντίδραση).