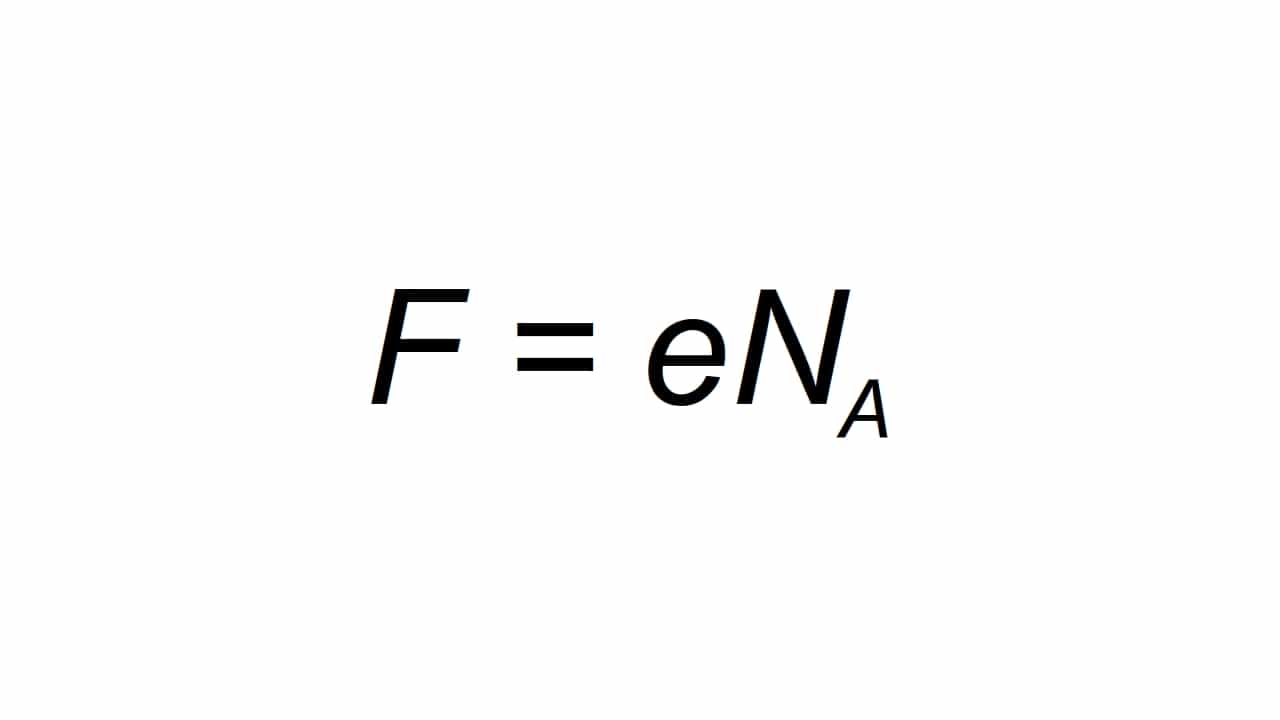Ahogy máskor is, az elektronika és a villamos energia területén más alapvető kérdéseket is kommentáltunk, mint pl Ohm törvénye, hullámok Kirchoff törvényei, sőt a alapvető elektromos áramkörök típusai, az is érdekes lenne tudni, hogy mi az Faraday állandó, mivel segíthet abban, hogy egy kicsit többet tudjon a terhelésekről.
Ebben a cikkben egy kicsit jobban megérti mi az állandó boldogság, mire lehet pályázni, és hogyan kell kiszámítani ...
Mi a Faraday -állandó?
La Faraday állandó a fizika és a kémia területén széles körben használt állandó. Ezt úgy határozzák meg, mint az elektromos töltés egy mól elektronra eső mennyiségét. Neve Michael Faraday brit tudósról származik. Ez az állandó felhasználható elektrokémiai rendszerekben az elektródában keletkező elemek tömegének kiszámításához.
Ezt betűvel lehet ábrázolni F, és a moláris elemi töltésként definiálják, hogy képes számol például:
lét F a kapott érték Farday -állandó, e az elemi elektromos töltés, és Na Avogadro állandója:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Az SI szerint ez a Faraday -állandó, mint más állandók, és pontos értéke: 96485,3321233100184 C / mol. Amint látja, C / mol egységben, azaz mólonként coulombokban fejezik ki. És hogy megértsük, melyek ezek az egységek, ha még nem tudja, akkor olvassa tovább a következő két részt ...
Mi az anyajegy?
Un mol egy egység, amely az anyag mennyiségét méri. Az egységek SI -n belül ez a 7 alapvető mennyiség egyike. Bármely anyagban, legyen az elem vagy kémiai vegyület, az elemi egységek sorozata alkotja. Egy vakond 6,022 140 76 × 10 -nek felel meg23 elemi entitások, amely az Avogadro állandó állandó számértéke.
Ezek az elemi entitások lehetnek atomok, molekulák, ionok, elektronok, fotonok vagy bármely más típusú elemi részecske. Például ezzel megteheti számolja ki az atomok számát mi van egy gramm adott anyagban.
Az kémia, a vakond elengedhetetlen, mivel lehetővé teszi számos számítás elvégzését összetételekre, kémiai reakciókra stb. Például víz esetén (H2O), van egy reakciód 2 H2 + VAGY2 → 2H2O, azaz két mól hidrogén (H2) és egy mól oxigént (O2) reagálva két mól vizet képez. Továbbá a koncentráció kifejezésére is használhatók (lásd a molaritást).
Mi az elektromos töltés?
Másrészt a elektromos töltés Más esetekben már beszéltünk, ez néhány szubatomi részecske belső fizikai tulajdonsága, amelyek az elektromágneses mezők miatt vonzó és taszító erőket mutatnak ki közöttük. A töltés és az elektromos mező közötti elektromágneses kölcsönhatás a fizika négy alapvető kölcsönhatásának egyike, az erős nukleáris erővel, a gyenge nukleáris erővel és a gravitációs erővel együtt.
Ennek az elektromos töltésnek a méréséhez a Coulomb (C) vagy Coulomb, és az egy amper erősségű elektromos áram által egy másodperc alatt szállított töltésmennyiség.
A Faraday -állandó alkalmazása

Ha vajon mi? praktikus alkalmazás Lehet ez a Faraday -állandó, az igazság az, hogy jó néhány van, néhány példa:
- Galvanizálás / eloxálás: a kohászati ipar olyan eljárásaihoz, ahol az egyik fémet elektrolízissel borítják a másikra. Például, ha az acélt horganyozzák egy cinkréteggel, hogy nagyobb ellenállást biztosítsanak a korrózióval szemben. Ezekben az eljárásokban a bevonandó fémet használják anódként, és az elektrolit az anód anyag oldható sója.
- Fém tisztítása: alkalmazható a fémek, például réz, cink, ón stb. Szintén elektrolízis eljárásokkal.
- Vegyi gyártás: kémiai vegyületek előállításához ezt az állandót is általában használják.
- Kémiai elemzés: elektrolízissel a kémiai összetétel is meghatározható.
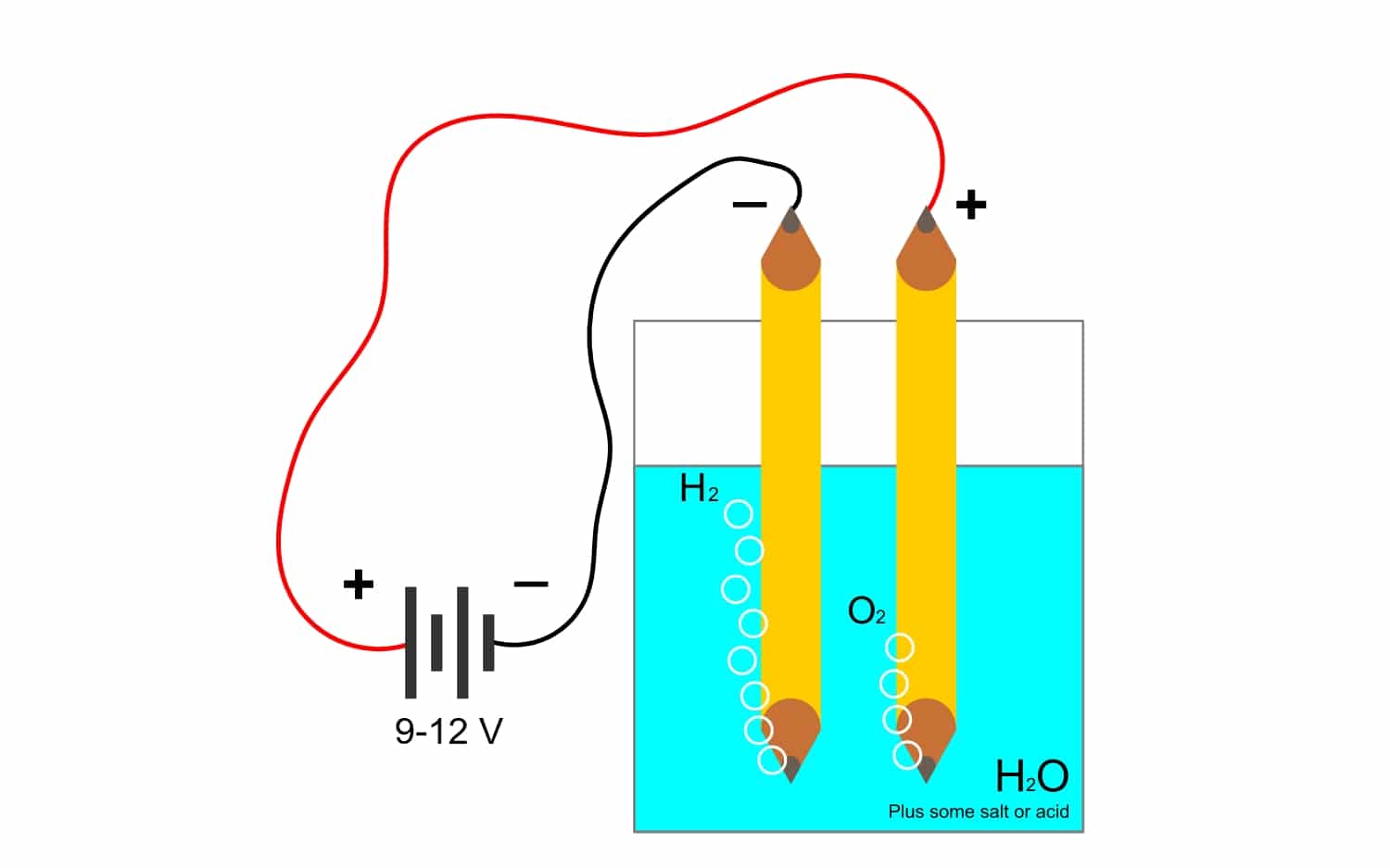
- Gáztermelés: a vízből elektrolízissel nyert gázok, például oxigén vagy hidrogén is ezt az állandót használják számításokhoz.
- Orvostudomány és esztétikaAz elektrolízis bizonyos idegek stimulálására vagy bizonyos problémák kezelésére is használható a nem kívánt szőr eltávolítása mellett. Az állandó nélkül az ilyen típusú eszközök sokaságát nem lehetett volna kifejleszteni.
- Nyomtatás: Nyomtatóknál bizonyos elemeknél elektrolízis folyamatokat is alkalmaznak.
- Elektrolit kondenzátorok: jól ismert elektronikai alkatrész, amely egy vékony alumínium-oxid fóliából és egy elektródák közötti alumínium-anódból áll. Az elektrolit bórsav, glicerin és ammónium -hidroxid keveréke. És így érik el ezeket a nagy kapacitásokat ...
Mi az elektrolízis?
És mivel a Faraday -állandó olyan szorosan összefügg a elektrolízisLássuk, mi ez a másik kifejezés, amelyet sokat használnak az iparban. Ennek a folyamatnak köszönhetően egy vegyület elemei elektromosan elkülöníthetők. Ez úgy történik, hogy az anódanionok elektronokat bocsátanak ki (oxidáció), és az elektronokat elfogják a katódkationok (redukció).
William Nicholson fedezte fel véletlenül, 1800 -ban, a vegyi elemek működésének tanulmányozása során. 1834 -ben, Michael Faraday kidolgozta és közzétette az elektrolízis törvényeit.
Például az elektrolízis víz H2O, lehetővé teszi oxigén és hidrogén előállítását. Ha egyenáramot alkalmaznak elektródákon keresztül, amely elválasztja az oxigént a hidrogéntől, és képes lesz mindkét gázt elkülöníteni (nem érintkezhetnek, mivel nagyon veszélyes robbanásveszélyes reakciót váltanak ki).