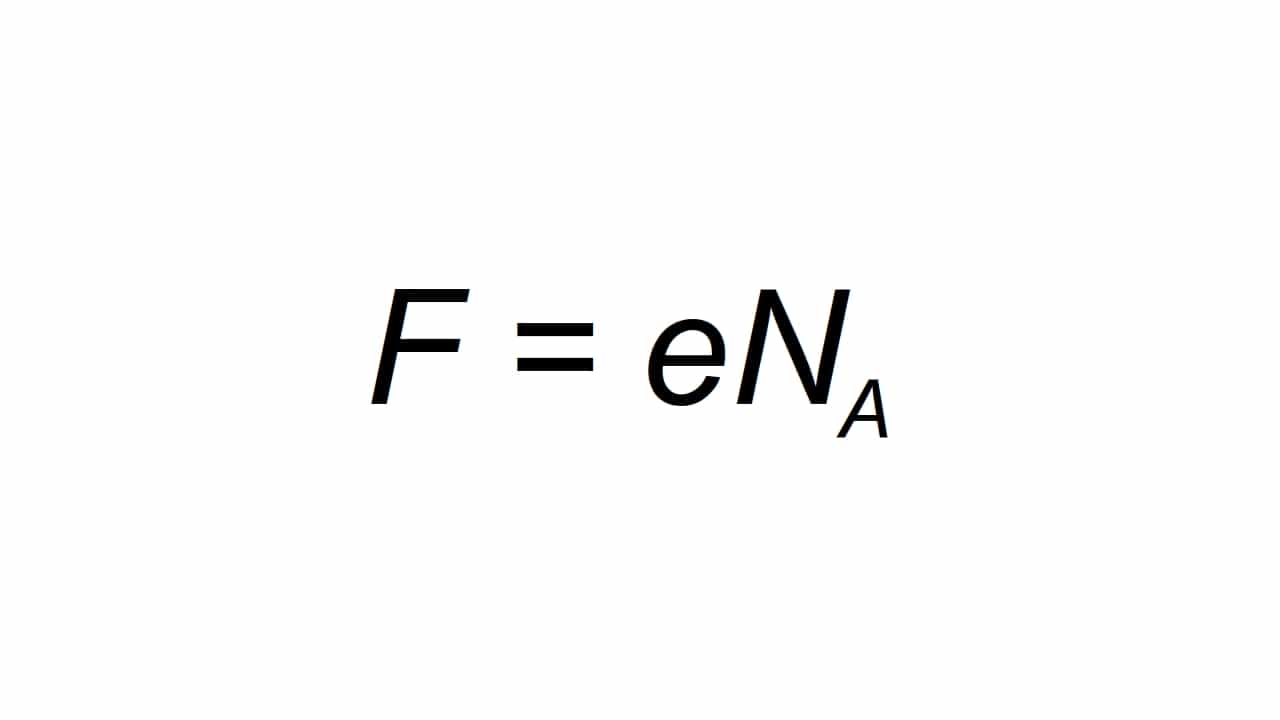כמו בזמנים אחרים הגענו לשאלות יסוד אחרות בתחום האלקטרוניקה והחשמל, כגון חוק אוהם, גלים חוקי קירצ'וף, ואפילו את סוגי מעגלים חשמליים בסיסיים, יהיה מעניין גם לדעת מה זה פאראדיי קבוע, מכיוון שהוא יכול לעזור לך לדעת קצת יותר על העומסים.
במאמר זה תבינו קצת יותר טוב מהו אושר מתמיד, על מה ניתן לבקש אותו, וכיצד הוא מחושב ...
מהו קבוע פאראדיי?
La פאראדיי קבוע זהו קבוע בשימוש נרחב בתחומי הפיזיקה והכימיה. הוא מוגדר ככמות המטען החשמלי לשומה של אלקטרונים. שמו בא מהמדען הבריטי מייקל פאראדיי. ניתן להשתמש בקבוע זה במערכות אלקטרוכימיות לחישוב מסת האלמנטים הנוצרים באלקטרודה.
זה יכול להיות מיוצג על ידי האות F, והוא מוגדר כמטען היסודי הטוחני, להיות מסוגל לחשב כמו:
להיות F הערך המתקבל מהקבוע של פרדיי, כלומר המטען החשמלי היסודי, ו- Na הוא הקבוע של אבוגדרו:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 M-1
על פי ה- SI, קבוע פאראדיי זה מדויק, כמו קבועים אחרים, וערכו המדויק הוא: 96485,3321233100184 C / mol. כפי שאתה יכול לראות, זה מתבטא ביחידה C / mol, כלומר, coulombs לכל שומה. וכדי להבין מהי יחידות אלו, אם אינך יודע עדיין, תוכל להמשיך לקרוא את שני הקטעים הבאים ...
מה זה שומה?
Un M היא יחידה המודדת את כמות החומר. בתוך SI של היחידות, הוא אחד משבעת הכמויות הבסיסיות. בכל חומר, בין אם זה יסוד או תרכובת כימית, יש סדרה של יחידות יסוד המרכיבות אותו. שומה אחת תהיה שווה ל 7 6,022 140 × 7623 ישויות יסודיות, שהוא הערך המספרי הקבוע של הקבוע של Avogadro.
ישויות יסוד אלה יכולות להיות אטום, מולקולה, יון, אלקטרון, פוטונים או כל סוג אחר של חלקיק יסודי. לדוגמה, בעזרת זה אתה יכול לחשב את מספר האטומים מה יש בגרם של חומר נתון.
ב כימיה, השומה חיונית, מכיוון שהיא מאפשרת לבצע חישובים רבים עבור קומפוזיציות, תגובות כימיות וכו '. לדוגמה, עבור מים (H2O), יש לך תגובה 2 H2 + O.2 → 2H2Oכלומר שני שומות של מימן (H2) ושומה אחת של חמצן (O2) מגיבים ליצירת שתי שומות מים. יתר על כן, ניתן להשתמש בהם גם להבעת ריכוז (ראה מולריות).
מהו המטען החשמלי?
מצד שני, מתוך מטען חשמלי כבר דיברנו בהזדמנויות אחרות, זהו מאפיין פיסי מהותי של חלקיקים תת -אטומיים המבטאים ביניהם כוחות משיכה ודוחה עקב שדות אלקטרומגנטיים. האינטראקציה האלקטרומגנטית, בין המטען לשדה החשמלי, היא אחת מ -4 האינטראקציות הבסיסיות בפיזיקה, יחד עם הכוח הגרעיני החזק, הכוח הגרעיני החלש וכוח הכבידה.
כדי למדוד מטען חשמלי זה, קולומב (ג) או קולומב, והוא מוגדר כמות המטען הנישאת בשנייה אחת על ידי זרם חשמלי בעוצמה אמפר אחד.
יישומים של קבוע פאראדיי

אם אתה תוהה מה יישום מעשי אתה יכול לקבל את קבוע פאראדיי הזה, האמת היא שיש לך לא מעט, כמה דוגמאות הן:
- ציפוי חשמל / אנודייז: לתהליכים בתעשיית המתכות שבה מתכת אחת מכוסה במתכת אחרת על ידי אלקטרוליזה. לדוגמה, כאשר הפלדה מגולוונת בשכבת אבץ כדי לתת לה עמידות רבה יותר בפני קורוזיה. בתהליכים אלה, המתכת שיש לציפוי משמשת כאנודה והאלקטרוליט הוא מלח מסיס של חומר האנודה.
- טיהור מתכת: ניתן ליישם אותו גם בנוסחאות המשמשות לעידון מתכות כגון נחושת, אבץ, פח וכו '. גם בהליכי אלקטרוליזה.
- ייצור כימי: לייצור תרכובות כימיות גם בדרך כלל משתמשים בקבוע הזה.
- ניתוח כימי: על ידי אלקטרוליזה ניתן גם לקבוע את ההרכב הכימי.
- ייצור גז: גזים כגון חמצן או מימן המתקבלים ממים באמצעות אלקטרוליזה משתמשים גם בקבוע זה לחישובים.
- רפואה ואסתטיקהאלקטרוליזה יכולה לשמש גם להמרצת עצבים מסוימים או לטיפול בבעיות מסוימות, בנוסף להסרת שיער לא רצוי. ללא הקבוע, לא ניתן היה לפתח מספר רב של כלים מסוג זה.
- דפס: עבור מדפסות, תהליכי אלקטרוליזה משמשים גם עבור אלמנטים מסוימים.
- קבלים אלקטרוליטיים: רכיב אלקטרוני ידוע המורכב מסרט דק של תחמוצת אלומיניום ואנודה מאלומיניום בין האלקטרודות. האלקטרוליט הוא תערובת של חומצה בורית, גליצרין ואמוניום הידרוקסיד. וכך מושגים היכולות הגדולות האלה ...
מהי אלקטרוליזה?
ומכיוון שקבוע פאראדיי קשור כל כך קרוב ל הַפרָדָה חַשְׁמָלִיתבואו נראה מהו המונח הנוסף הזה המשמש הרבה בתעשייה. הודות לתהליך זה ניתן להפריד אלמנטים של תרכובת באמצעות חשמל. הדבר נעשה על ידי שחרור אלקטרונים על ידי אניוני האנודה (חמצון) ולכידת אלקטרונים על ידי קטיוני הקתודה (צמצום).
הוא התגלה בטעות על ידי ויליאם ניקולסון, בשנת 1800, בעת לימוד הפעולה של סוללות כימיות. בשנת 1834, מייקל פאראדיי פיתח ופרסם את חוקי האלקטרוליזה.
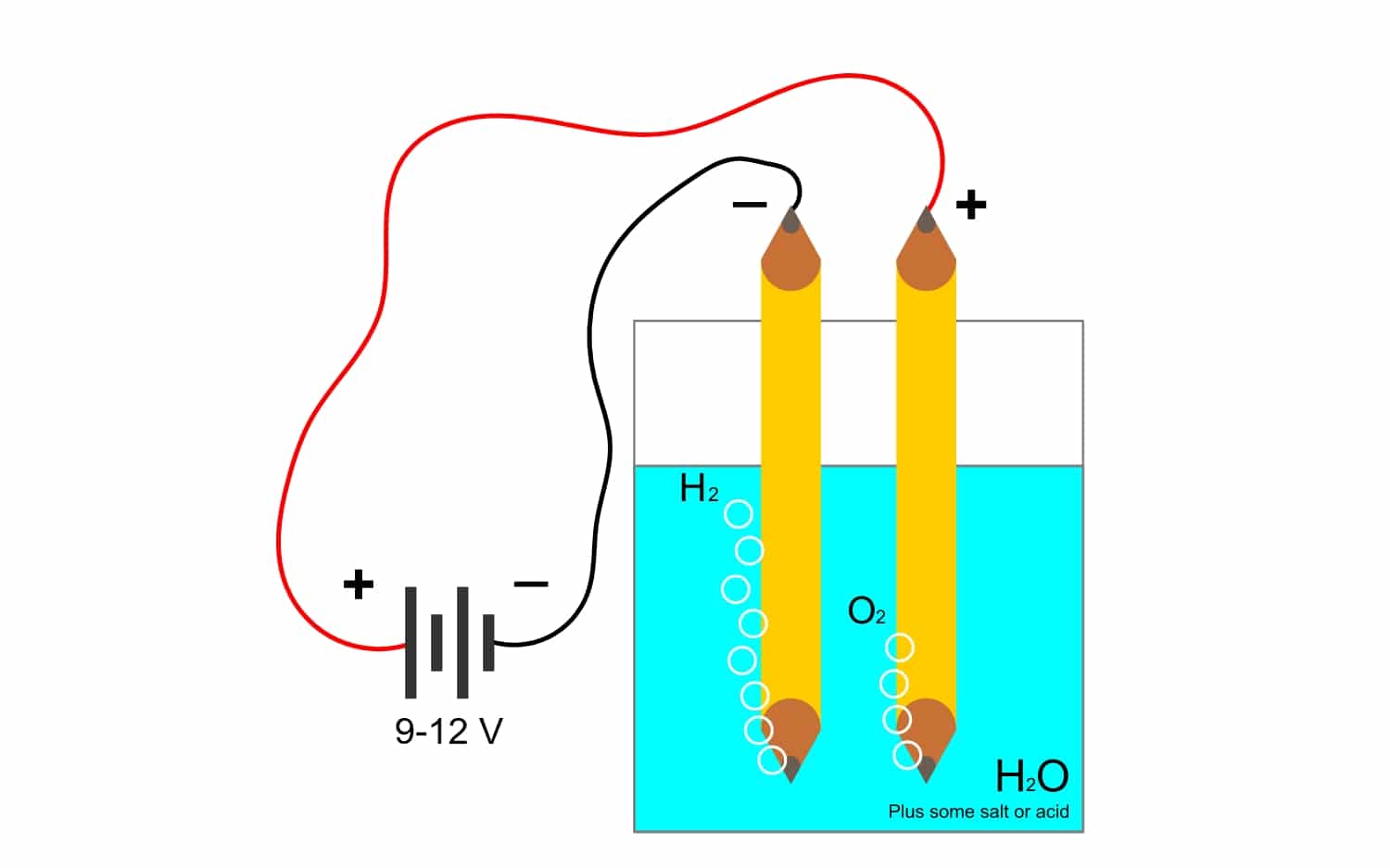
לדוגמה, אלקטרוליזה של מים ח2O, מאפשר ליצור חמצן ומימן. אם מופעל זרם ישיר באמצעות אלקטרודות, שיפרידו בין החמצן למימן, ויוכלו לבודד את שני הגזים (הם לא יכולים לבוא במגע, מכיוון שהם מייצרים תגובה נפץ מסוכנת מאוד).