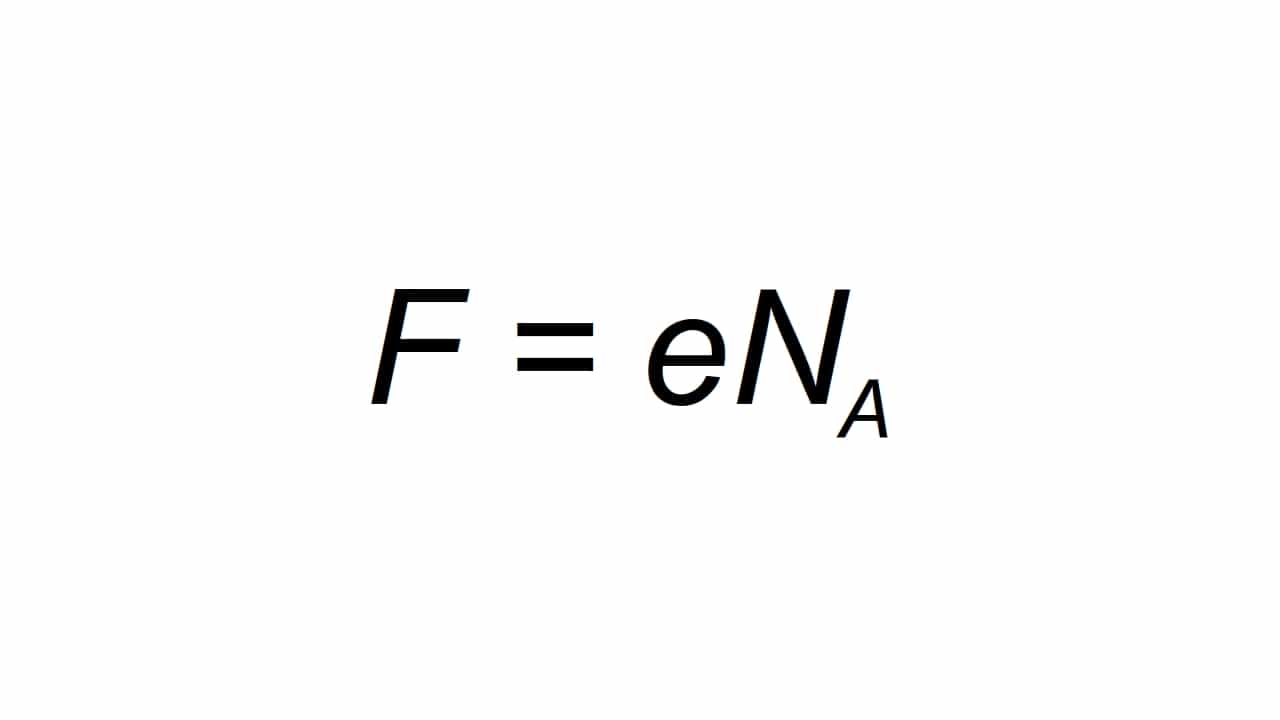Tāpat kā citas reizes, mēs esam komentējuši citus pamatjautājumus elektronikas un elektrības jomā, piemēram, Oma likums, viļņi Kirhofa likumi, un pat pamata elektrisko ķēžu veidi, būtu arī interesanti uzzināt, kas tas ir Faradeja konstante, jo tas var palīdzēt jums uzzināt nedaudz vairāk par slodzēm.
Šajā rakstā jūs sapratīsit nedaudz labāk kas ir pastāvīga svētlaime, uz ko to var pieteikties un kā to aprēķināt ...
Kas ir Faraday konstante?
La Faradeja konstante tā ir konstante, ko plaši izmanto fizikas un ķīmijas jomās. To definē kā elektriskā lādiņa daudzumu uz vienu elektronu molu. Tās nosaukums cēlies no britu zinātnieka Maikla Faradeja. Šo konstanti var izmantot elektroķīmiskajās sistēmās, lai aprēķinātu elektrodu veidojošo elementu masu.
To var attēlot ar burtu F, un tiek definēts kā molārā elementārā lādiņa spēja aprēķināt kā:
Būt F iegūto vērtību no Fārdeja konstantes, piemēram, elementārā elektriskā lādiņa, un Na ir Avogadro konstante:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Saskaņā ar SI, šī Faraday konstante ir precīza, tāpat kā citas konstantes, un tās precīza vērtība ir: 96485,3321233100184 C / mol. Kā redzat, tas ir izteikts vienībā C / mol, tas ir, kuloni uz molu. Un, lai saprastu, kas ir šīs vienības, ja vēl nezināt, varat turpināt lasīt nākamās divas sadaļas ...
Kas ir mols?
Un mol ir vienība, kas mēra vielas daudzumu. Vienību SI robežās tas ir viens no 7 pamata lielumiem. Jebkurā vielā, vai tas būtu elements vai ķīmisks savienojums, ir virkne elementāru vienību, kas to veido. Viens mols būtu līdzvērtīgs 6,022 140 76 × 1023 elementāras entītijas, kas ir Avogadro konstantes fiksētā skaitliskā vērtība.
Šīs elementu vienības var būt atoms, molekula, jons, elektrons, fotoni vai jebkura cita veida elementārdaļiņa. Piemēram, ar šo jūs varat aprēķiniet atomu skaitu kas ir gramā dotās vielas.
Jo ķīmija, mols ir būtisks, jo tas ļauj veikt daudzus aprēķinus par kompozīcijām, ķīmiskajām reakcijām utt. Piemēram, ūdenim (H.2O), jums ir reakcija 2 H2 + VAI2 → 2 H2O, tas ir, ka divi moli ūdeņraža (H2) un vienu molu skābekļa (O2) reaģē, veidojot divus molu ūdens. Turklāt tos var izmantot arī, lai izteiktu koncentrāciju (sk. Molaritāti).
Kas ir elektriskais lādiņš?
No otras puses, no elektriskais lādiņš Mēs jau esam runājuši citos gadījumos, tā ir dažu subatomisko daļiņu raksturīga fiziska īpašība, kas elektromagnētisko lauku dēļ rada pievilcīgus un atbaidošus spēkus. Elektromagnētiskā mijiedarbība starp lādiņu un elektrisko lauku ir viena no četrām fizikas pamatmijiedarbībām kopā ar spēcīgu kodolspēku, vāju kodolspēku un gravitācijas spēku.
Lai izmērītu šo elektrisko lādiņu, Kulons (C) vai Kulons, un to definē kā lādiņa daudzumu, ko vienā sekundē pārnes elektriskā strāva ar vienu ampēru.
Faraday konstantes pielietojumi

Ja jums rodas jautājums par ko praktisks pielietojums Jums var būt šī Faraday konstante, patiesība ir tāda, ka jums ir diezgan daudz, daži piemēri:
- Galvanizācija / anodēšana: procesiem metalurģijas nozarē, kur viens metāls ir pārklāts ar citu elektrolīzes ceļā. Piemēram, ja tērauds tiek cinkots ar cinka slāni, lai tam būtu lielāka izturība pret koroziju. Šajos procesos pārklājamais metāls tiek izmantots kā anods, un elektrolīts ir anoda materiāla šķīstošs sāls.
- Metāla attīrīšana: to var attiecināt arī uz formulām, ko izmanto metālu, piemēram, vara, cinka, alvas, uzlabošanai. Arī ar elektrolīzes procedūrām.
- Ķīmiskā ražošana: šo ķīmisko savienojumu ražošanai parasti izmanto arī šo konstanti.
- Ķīmiskā analīze: ar elektrolīzi var noteikt arī ķīmisko sastāvu.
- Gāzes ražošana: gāzes, piemēram, skābeklis vai ūdeņradis, ko iegūst no ūdens elektrolīzes ceļā, arī izmanto šo konstanti aprēķinos.
- Medicīna un estētikaElektrolīzi var izmantot arī, lai stimulētu noteiktus nervus vai ārstētu noteiktas problēmas, turklāt noņemot nevēlamus matiņus. Bez konstantes daudzus šāda veida rīkus nevarētu izstrādāt.
- Drukāt: Printeriem elektrolīzes procesus izmanto arī atsevišķiem elementiem.
- Elektrolītiskie kondensatori: plaši pazīstama elektroniska sastāvdaļa, kas sastāv no plānas alumīnija oksīda plēves un alumīnija anoda starp elektrodiem. Elektrolīts ir borskābes, glicerīna un amonija hidroksīda maisījums. Un tā tiek sasniegtas šīs lieliskās spējas ...
Kas ir elektrolīze?
Un tā kā Faraday konstante ir tik cieši saistīta ar elektrolīzeApskatīsim, kāds ir šis cits termins, ko šajā nozarē lieto daudz. Pateicoties šim procesam, savienojuma elementus var atdalīt ar elektrību. To veic, anoda anjoniem atbrīvojot elektronus (oksidēšanās) un elektronus uztverot ar katoda katjoniem (reducēšana).
To nejauši atklāja Viljams Nikolsons, 1800. gadā, pētot ķīmisko bateriju darbību. 1834. gadā Maikls Faradejs izstrādāja un publicēja elektrolīzes likumus.
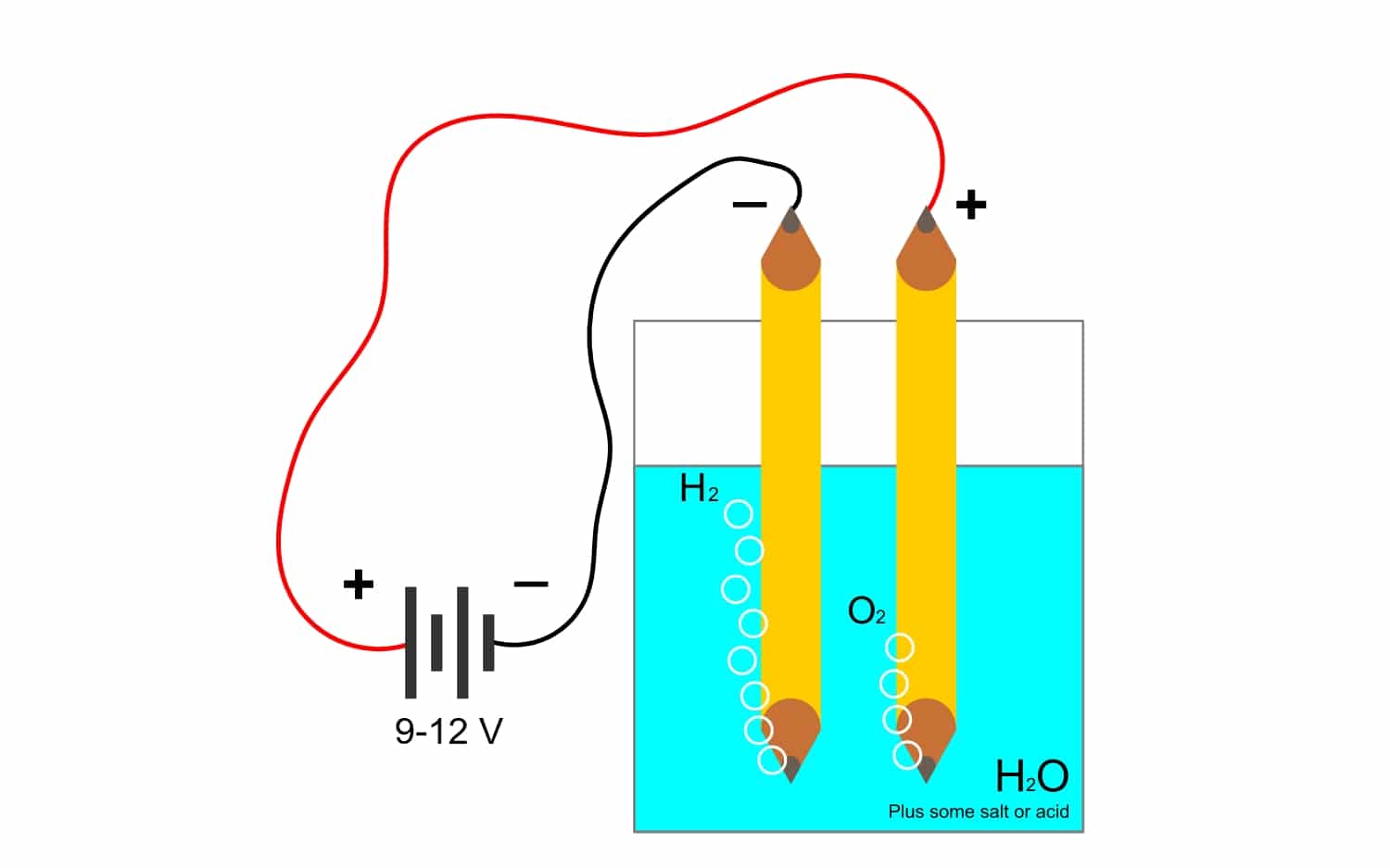
Piemēram, elektrolīze ūdens H2O, ļauj radīt skābekli un ūdeņradi. Ja caur elektrodiem tiek pielietota līdzstrāva, kas atdalīs skābekli no ūdeņraža un spēs izolēt abas gāzes (tās nevar saskarties, jo rada ļoti bīstamu sprādzienbīstamu reakciju).