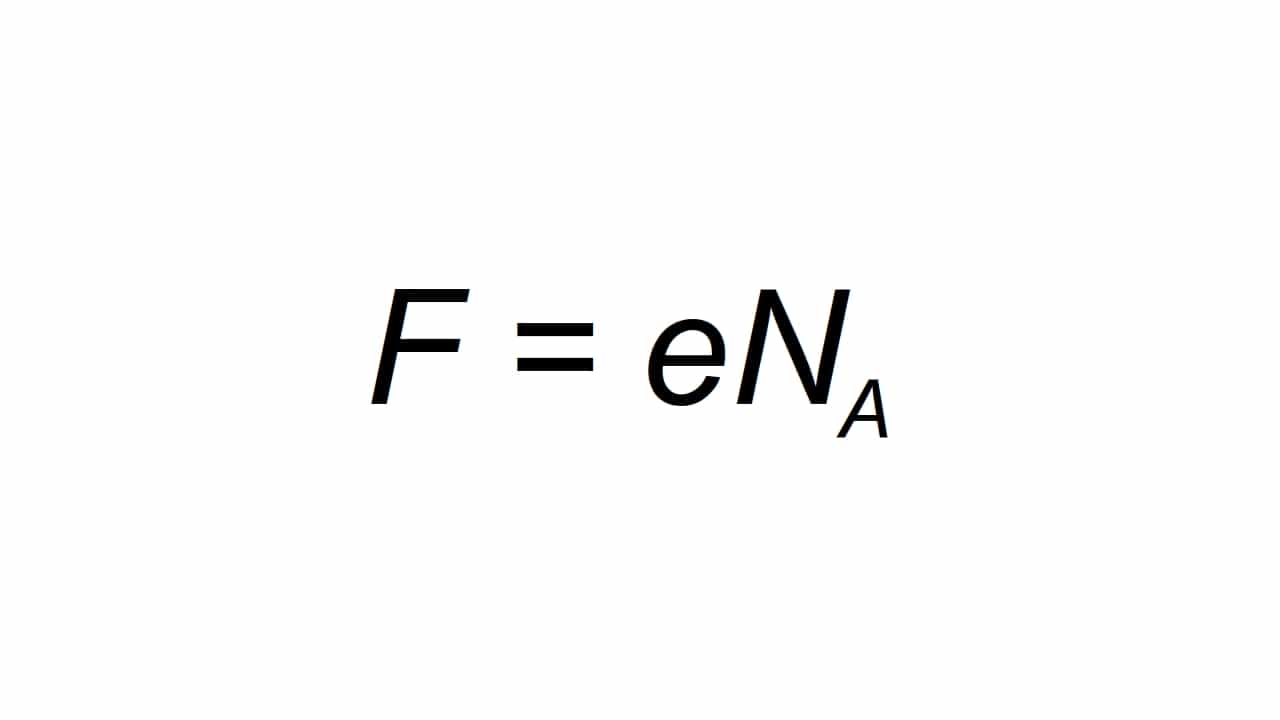Net als andere keren hebben we opmerkingen gemaakt over andere fundamentele vragen op het gebied van elektronica en elektriciteit, zoals: De wet van Ohmof de De wetten van Kirchoff, en zelfs de soorten elektrische basiscircuits, zou het ook interessant zijn om te weten wat het is Constante van Faraday, omdat het u kan helpen iets meer te weten over de ladingen.
In dit artikel zul je het een beetje beter begrijpen wat is constante gelukzaligheid?, wat kan het worden aangevraagd en hoe wordt het berekend ...
Wat is de constante van Faraday?
La Constante van Faraday het is een constante die veel wordt gebruikt op het gebied van natuurkunde en scheikunde. Het wordt gedefinieerd als de hoeveelheid elektrische lading per mol elektronen. De naam komt van de Britse wetenschapper Michael Faraday. Deze constante kan in elektrochemische systemen worden gebruikt om de massa te berekenen van de elementen die zich in een elektrode vormen.
Het kan worden weergegeven door de letter F, en wordt gedefinieerd als de molaire elementaire lading, in staat Calcular als:
zijnde F de resulterende waarde van de constante van Farday, e de elementaire elektrische lading, en Na is de constante van Avogadro:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Volgens de SI is deze constante van Faraday exact, net als andere constanten, en de precieze waarde is: 96485,3321233100184 C / mol. Zoals u kunt zien, wordt het uitgedrukt in de eenheid C / mol, dat wil zeggen coulombs per mol. En om te begrijpen wat deze eenheden zijn, kunt u, als u het nog niet weet, doorgaan met het lezen van de volgende twee secties ...
Wat is een mol?
Un mol is een eenheid die de hoeveelheid stof meet. Binnen de SI van eenheden is het een van de 7 fundamentele grootheden. In elke stof, of het nu een element of een chemische verbinding is, zijn er een reeks elementaire eenheden waaruit het bestaat. Eén mol zou gelijk zijn aan 6,022 140 76 × 1023 elementaire entiteiten, wat de vaste numerieke waarde is van de constante van Avogadro.
Deze elementaire entiteiten kunnen een atoom, een molecuul, een ion, een elektron, fotonen of elk ander type elementair deeltje zijn. Hiermee kunt u bijvoorbeeld: bereken het aantal atomen wat er in een gram van een bepaalde stof zit.
In de chemie, is de mol essentieel, omdat hiermee veel berekeningen kunnen worden gemaakt voor composities, chemische reacties, enz. Bijvoorbeeld voor water (H2O), je hebt een reactie 2 H2 + OF2 → 2H2O, dat wil zeggen, dat twee mol waterstof (H2) en één mol zuurstof (O2) reageren om twee mol water te vormen. Bovendien kunnen ze ook worden gebruikt om concentratie uit te drukken (zie molariteit).
Wat is de elektrische lading?
Aan de andere kant, van de elektrische lading We hebben al bij andere gelegenheden gesproken, het is een intrinsieke fysieke eigenschap van sommige subatomaire deeltjes die door elektromagnetische velden aantrekkende en afstotende krachten vertonen. De elektromagnetische interactie, tussen de lading en het elektrische veld, is een van de 4 fundamentele interacties in de natuurkunde, samen met de sterke kernkracht, de zwakke kernkracht en de zwaartekracht.
Om deze elektrische lading te meten, Coulomb (C) of Coulomb, en wordt gedefinieerd als de hoeveelheid lading die in één seconde wordt gedragen door een elektrische stroom met een intensiteit van één ampère.
Toepassingen van de constante van Faraday

Als je je afvraagt wat praktische toepassing Je kunt deze constante van Faraday hebben, de waarheid is dat je er nogal wat hebt, enkele voorbeelden zijn:
- Galvaniseren / anodiseren: voor processen in de metallurgische industrie waarbij het ene metaal door middel van elektrolyse met het andere wordt bedekt. Bijvoorbeeld wanneer staal wordt gegalvaniseerd met een laag zink om het beter bestand te maken tegen corrosie. Bij deze processen wordt het te bekleden metaal als anode gebruikt en is de elektrolyt een oplosbaar zout van het anodemateriaal.
- Metaalzuivering: het kan ook worden toegepast op de formules die worden gebruikt voor de verfijning van metalen zoals koper, zink, tin, enz. Ook door elektrolyseprocedures.
- Chemische productie: om chemische verbindingen te produceren wordt deze constante meestal ook gebruikt.
- Chemische analyse: door middel van elektrolyse kon ook de chemische samenstelling worden bepaald.
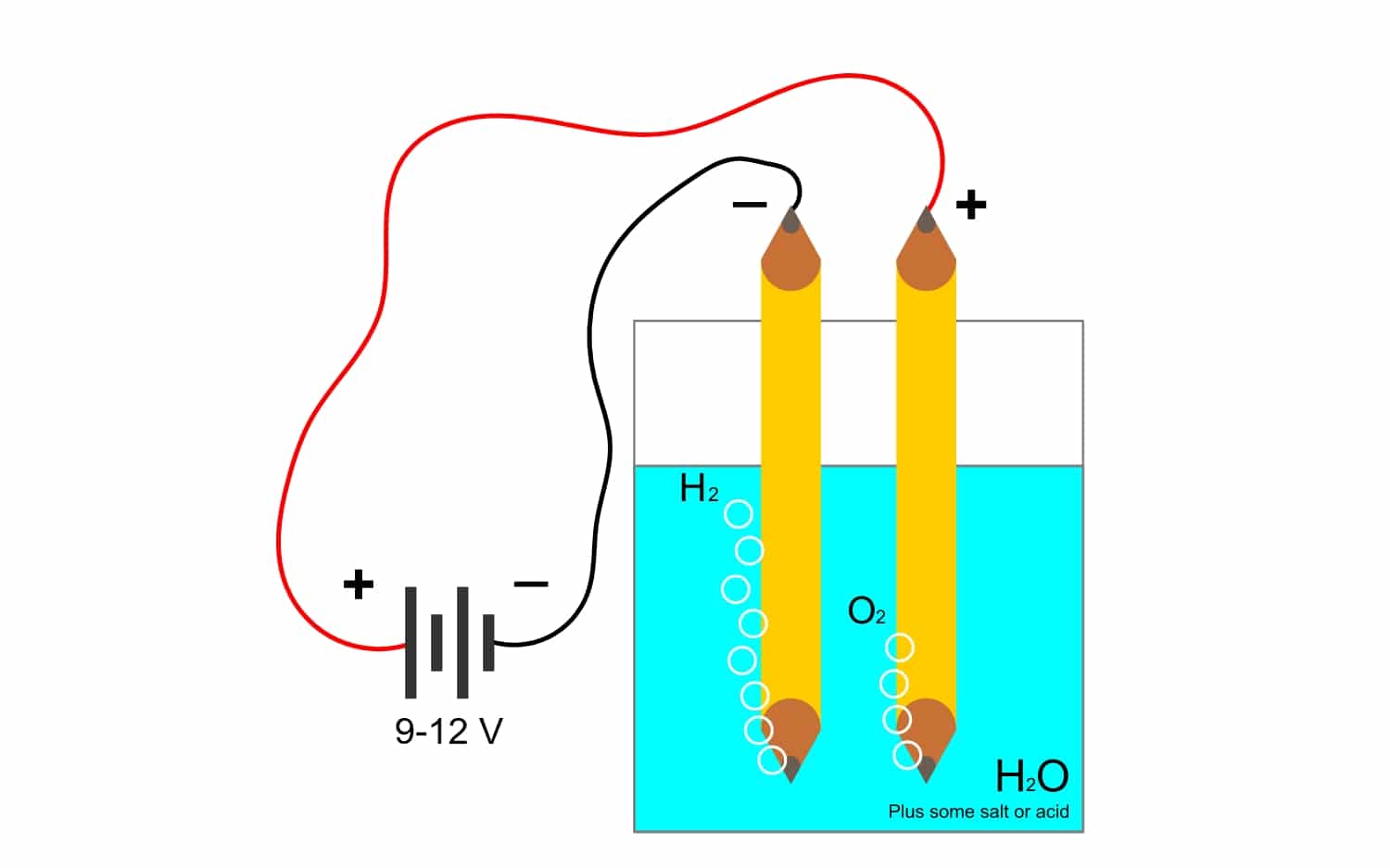
- Gasproductie: gassen zoals zuurstof of waterstof die door elektrolyse uit water worden gewonnen, gebruiken deze constante ook voor berekeningen.
- Geneeskunde en esthetiekNaast het verwijderen van ongewenst haar kan elektrolyse ook worden gebruikt om bepaalde zenuwen te stimuleren of bepaalde problemen te behandelen. Zonder de constante zou een veelvoud aan instrumenten van dit type niet zijn ontwikkeld.
- Afdrukken: Voor printers worden voor bepaalde elementen ook elektrolyseprocessen gebruikt.
- Elektrolytische condensatoren: een bekende elektronische component bestaande uit een dunne film van aluminiumoxide en een aluminiumanode tussen elektroden. De elektrolyt is een mengsel van boorzuur, glycerine en ammoniumhydroxide. En zo worden die grote capaciteiten bereikt...
Wat is elektrolyse?
En aangezien de constante van Faraday zo nauw verwant is aan de elektrolyseLaten we eens kijken wat deze andere term is die veel in de industrie wordt gebruikt. Dankzij dit proces kunnen elementen van een verbinding worden gescheiden door middel van elektriciteit. Dit gebeurt door het vrijkomen van elektronen door de anode-anionen (oxidatie) en het invangen van elektronen door de kathodekationen (reductie).
Het werd bij toeval ontdekt door William Nicholson, in 1800, terwijl hij de werking van chemische batterijen bestudeerde. in 1834, Michael Faraday ontwikkelde en publiceerde de wetten van elektrolyse.
Bijvoorbeeld elektrolyse van water H2O, maakt het mogelijk om zuurstof en waterstof te creëren. Als er een gelijkstroom wordt aangelegd door elektroden, die de zuurstof van de waterstof scheiden en beide gassen kunnen isoleren (ze kunnen niet met elkaar in contact komen, omdat ze een zeer gevaarlijke explosieve reactie veroorzaken).