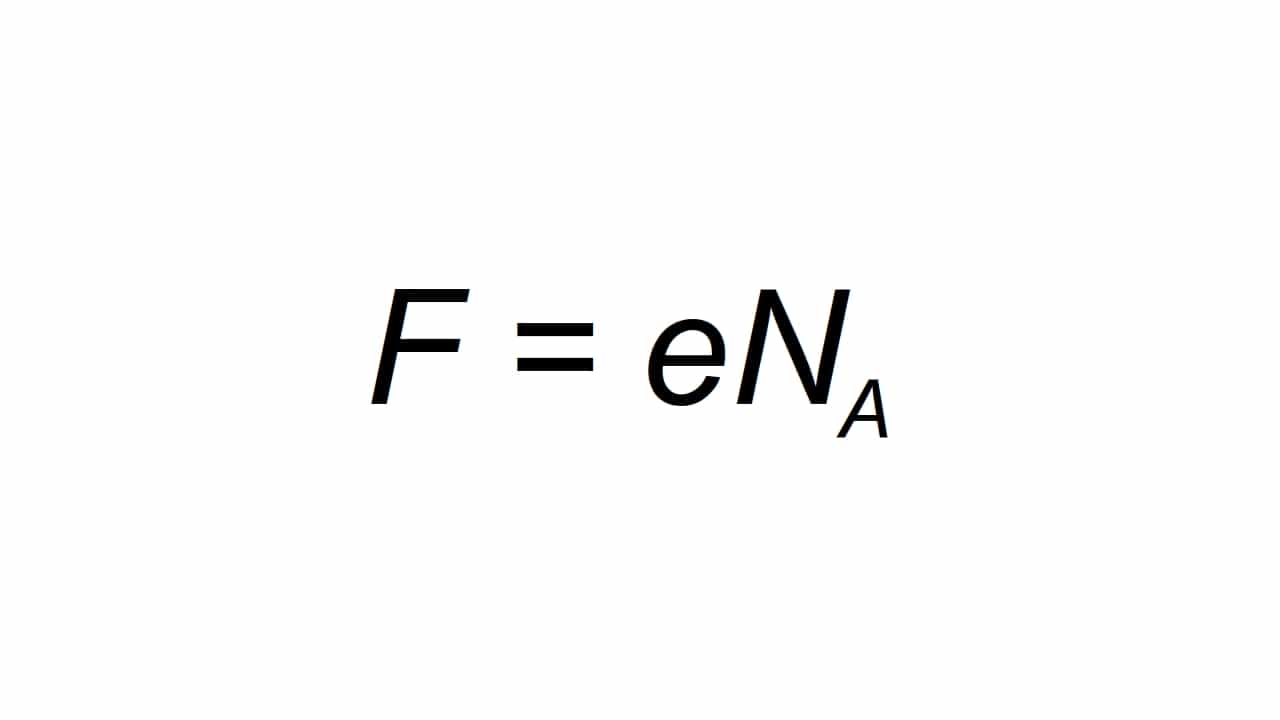Como em outras ocasiões, comentamos outras questões fundamentais no campo da eletrônica e da eletricidade, como o Lei de ohm, Ou o Leis de Kirchoff, e até mesmo o tipos de circuitos elétricos básicos, também seria interessante saber o que é Constante de Faraday, pois pode te ajudar a saber um pouco mais sobre as cargas.
Neste artigo você entenderá um pouco melhor o que é felicidade constante, o que pode ser aplicado e como é calculado ...
Qual é a constante de Faraday?
La Constante de Faraday é uma constante amplamente utilizada nas áreas de física e química. É definido como a quantidade de carga elétrica por mol de elétrons. Seu nome vem do cientista britânico Michael Faraday. Essa constante pode ser usada em sistemas eletroquímicos para calcular a massa dos elementos que se formam em um eletrodo.
Pode ser representado pela letra F, e é definido como a carga elementar molar, podendo calcular como:
Sendo F o valor resultante da constante de Farday, e a carga elétrica elementar, e Na é a constante de Avogadro:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
De acordo com o SI, esta constante de Faraday é exata, como outras constantes, e seu valor preciso é: 96485,3321233100184 C / mol. Como você pode ver, ele é expresso na unidade C / mol, ou seja, coulombs por mol. E para entender o que são essas unidades, se você ainda não sabe, pode continuar lendo as próximas duas seções ...
O que é uma toupeira?
Un mol é uma unidade que mede a quantidade de substância. Dentro do SI de unidades, é uma das 7 grandezas fundamentais. Em qualquer substância, seja um elemento ou um composto químico, há uma série de unidades elementares que a compõem. Um mol seria equivalente a 6,022 140 76 × 1023 entidades elementares, que é o valor numérico fixo da constante de Avogadro.
Essas entidades elementares podem ser um átomo, uma molécula, um íon, um elétron, fótons ou qualquer outro tipo de partícula elementar. Por exemplo, com isso você pode calcule o número de átomos o que está em um grama de uma determinada substância.
Em química, a toupeira é essencial, pois permite que muitos cálculos sejam feitos para composições, reações químicas, etc. Por exemplo, para água (H2O), você tem uma reação 2 H2 + O2 → 2H2O, isto é, que dois moles de hidrogênio (H2) e um mol de oxigênio (O2) reagem para formar dois moles de água. Além disso, eles também podem ser usados para expressar concentração (ver molaridade).
Qual é a carga elétrica?
Por outro lado, do carga elétrica Já falamos em outras ocasiões, é uma propriedade física intrínseca de algumas partículas subatômicas que manifestam forças de atração e repulsão entre si devido aos campos eletromagnéticos. A interação eletromagnética, entre a carga e o campo elétrico, é uma das 4 interações fundamentais na física, junto com a força nuclear forte, a força nuclear fraca e a força gravitacional.
Para medir essa carga elétrica, o Coulomb (C) ou Coulomb, e é definido como a quantidade de carga transportada em um segundo por uma corrente elétrica de intensidade um ampere.
Aplicações da constante de Faraday

Se você quer saber o que aplicação prática Você pode ter essa constante de Faraday, a verdade é que você tem alguns, alguns exemplos são:
- Galvanoplastia / anodização: para processos na indústria metalúrgica em que um metal é coberto com outro por eletrólise. Por exemplo, quando o aço é galvanizado com uma camada de zinco para dar maior resistência à corrosão. Nestes processos, o metal a ser revestido é usado como ânodo e o eletrólito é um sal solúvel do material do ânodo.
- Purificação de metal: também pode ser aplicado às fórmulas utilizadas para o refinamento de metais como cobre, zinco, estanho, etc. Também por procedimentos de eletrólise.
- Manufatura química: para produzir compostos químicos esta constante também é normalmente usada.
- Análises químicas: por eletrólise, a composição química também pode ser determinada.
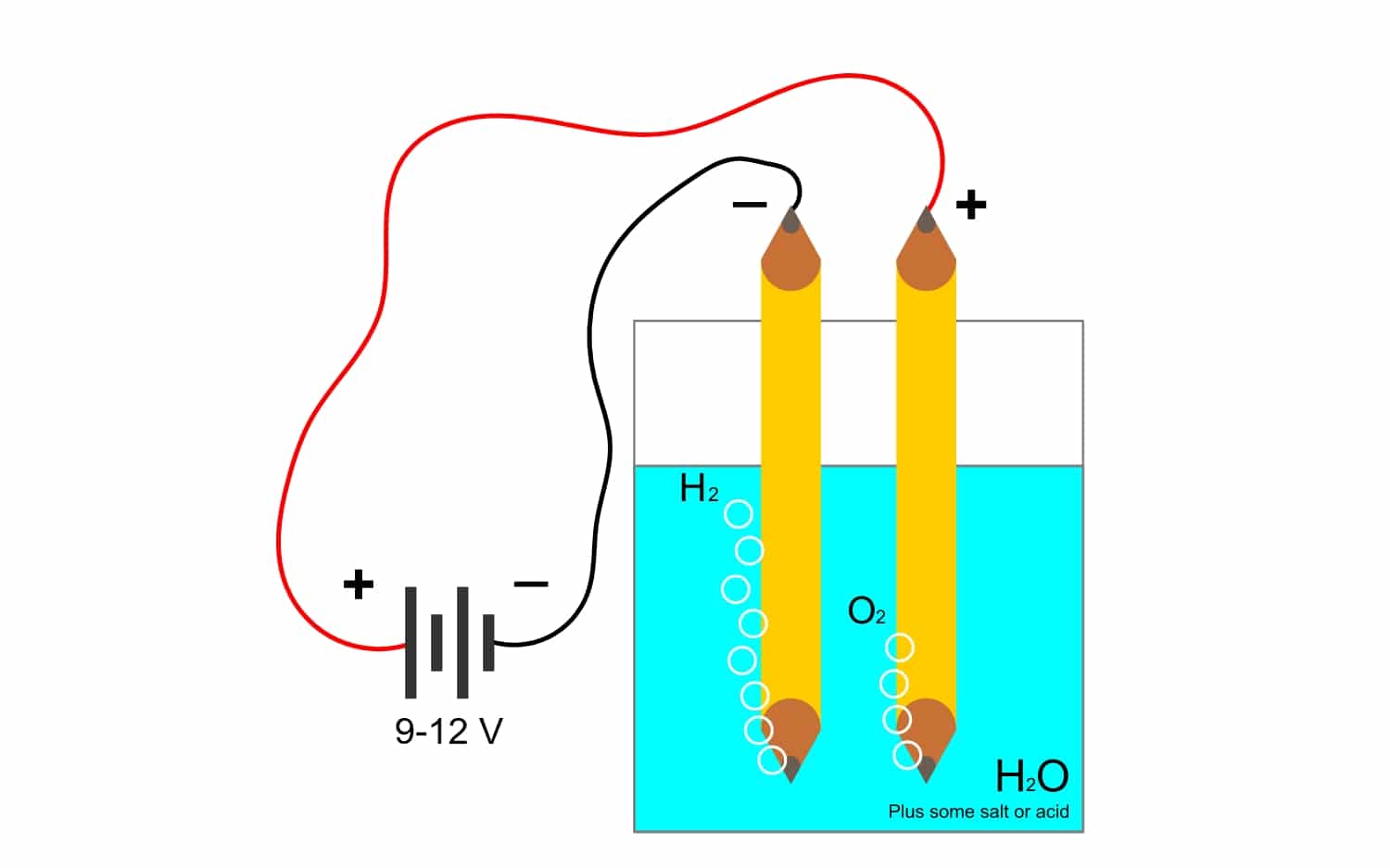
- Produção de gás: gases como oxigênio ou hidrogênio que são obtidos da água por eletrólise também usam essa constante para cálculos.
- Medicina e estéticaA eletrólise também pode ser usada para estimular certos nervos ou tratar certos problemas, além de remover pelos indesejáveis. Sem a constante, uma infinidade de ferramentas desse tipo não poderia ter sido desenvolvida.
- Imprimir: Para impressoras, os processos de eletrólise também são usados para certos elementos.
- Capacitores eletrolíticos: um conhecido componente eletrônico que consiste em uma fina película de óxido de alumínio e um ânodo de alumínio entre os eletrodos. O eletrólito é uma mistura de ácido bórico, glicerina e hidróxido de amônio. E é assim que essas grandes capacidades são alcançadas ...
O que é eletrólise?
E uma vez que a constante de Faraday está tão intimamente relacionada com o eletróliseVamos ver qual é esse outro termo que é muito usado na indústria. Graças a este processo, os elementos de um composto podem ser separados por meio de eletricidade. Isso é feito pela liberação de elétrons pelos ânions anódicos (oxidação) e pela captura de elétrons pelos cátions catódicos (redução).
Foi descoberto acidentalmente por William Nicholson, em 1800, enquanto estudava o funcionamento de baterias químicas. Em 1834, Michael Faraday desenvolveu e publicou as leis da eletrólise.
Por exemplo, a eletrólise de água H2O, permite criar oxigênio e hidrogênio. Se for aplicada uma corrente contínua através de eletrodos, que irá separar o oxigênio do hidrogênio, e será capaz de isolar os dois gases (eles não podem entrar em contato, pois produzem uma reação explosiva muito perigosa).