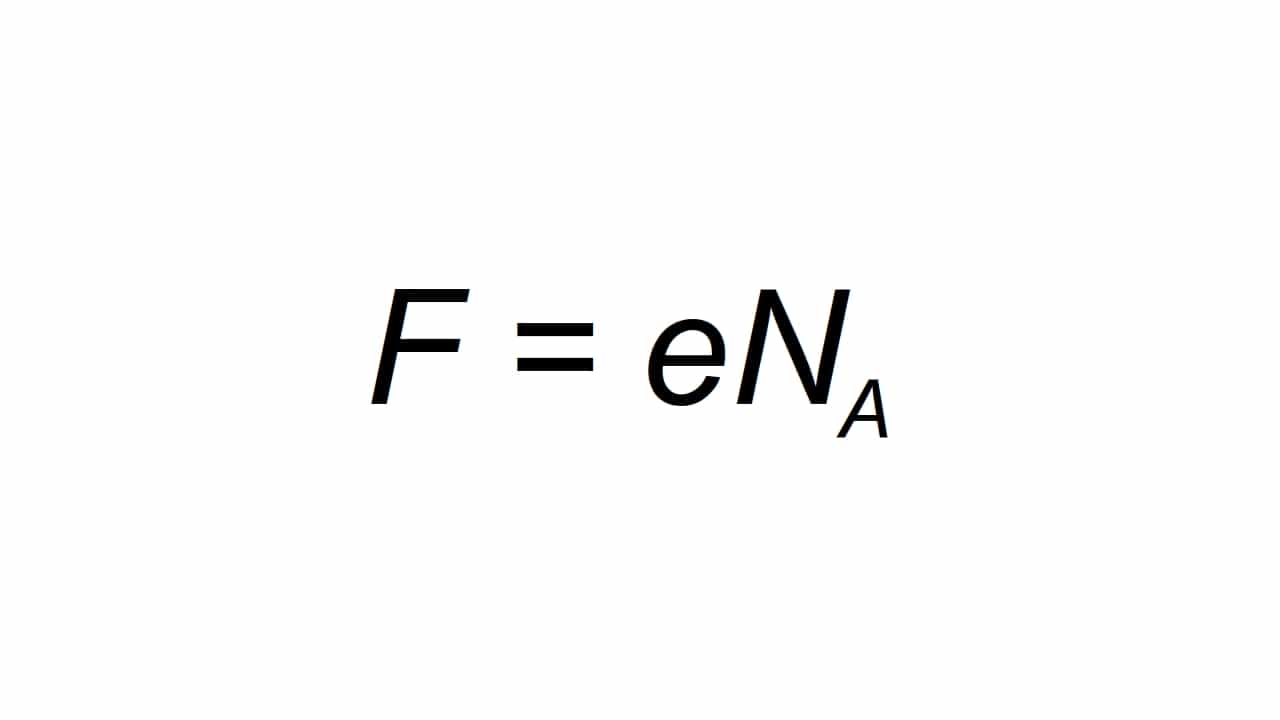La fel ca alteori, am comentat alte întrebări fundamentale din domeniul electronicii și al electricității, cum ar fi Legea lui Ohm, valuri Legile lui Kirchoff, și chiar tipuri de circuite electrice de bază, ar fi, de asemenea, interesant să știm ce este Constanta lui Faraday, deoarece vă poate ajuta să aflați mai multe despre încărcături.
În acest articol veți înțelege puțin mai bine ce este fericirea constantă, la ce se poate aplica și cum se calculează ...
Care este constanta Faraday?
La Constanta lui Faraday este o constantă utilizată pe scară largă în domeniile fizicii și chimiei. Este definit ca cantitatea de încărcare electrică per mol de electroni. Numele său provine de la savantul britanic Michael Faraday. Această constantă poate fi utilizată în sistemele electrochimice pentru a calcula masa elementelor care se formează într-un electrod.
Poate fi reprezentat prin scrisoare F, și este definit ca sarcina elementară molară, fiind capabil Calculeaza ca:
ființă F valoarea rezultată a constantei lui Farday, e sarcina electrică elementară, iar Na este constanta lui Avogadro:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Conform SI, această constantă Faraday este exactă, ca și alte constante, iar valoarea sa precisă este: 96485,3321233100184 C / mol. După cum puteți vedea, este exprimat în unitatea C / mol, adică coulombi pe mol. Și pentru a înțelege care sunt aceste unități, dacă nu știți încă, puteți continua să citiți următoarele două secțiuni ...
Ce este o aluniță?
Un mol este o unitate care măsoară cantitatea de substanță. În SI de unități, este una dintre cele 7 mărimi fundamentale. În orice substanță, indiferent dacă este un element sau un compus chimic, există o serie de unități elementare care o compun. Un mol ar fi echivalent cu 6,022 140 76 × 1023 entități elementare, care este valoarea numerică fixă a constantei lui Avogadro.
Aceste entități elementare pot fi un atom, o moleculă, un ion, un electron, fotoni sau orice alt tip de particulă elementară. De exemplu, cu aceasta poți calculați numărul de atomi ce este într-un gram dintr-o substanță dată.
În chimie, alunița este fundamentală, deoarece permite efectuarea a numeroase calcule pentru compoziții, reacții chimice etc. De exemplu, pentru apă (H2O), ai o reacție 2 H2 + SAU2 → 2 ore2O, adică doi moli de hidrogen (H2) și un mol de oxigen (O2) reacționează pentru a forma doi moli de apă. Mai mult, pot fi folosite și pentru exprimarea concentrației (a se vedea molaritatea).
Care este sarcina electrică?
Pe de altă parte, din incarcare electrica Am vorbit deja cu alte ocazii, este o proprietate fizică intrinsecă a unor particule subatomice care manifestă forțe atractive și respingătoare între ele datorită câmpurilor electromagnetice. Interacțiunea electromagnetică, între sarcină și câmpul electric, este una dintre cele 4 interacțiuni fundamentale din fizică, împreună cu forța nucleară puternică, forța nucleară slabă și forța gravitațională.
Pentru a măsura această încărcare electrică, Coulomb (C) sau Coulomb, și este definit ca cantitatea de încărcare purtată într-o secundă de un curent electric de intensitate de un amper.
Aplicații ale constantei Faraday

Dacă vă întrebați ce aplicație practică Puteți avea această constantă Faraday, adevărul este că aveți destul de multe, câteva exemple sunt:
- Galvanizare / anodizare: pentru procese din industria metalurgică în care un metal este acoperit cu altul prin electroliză. De exemplu, atunci când oțelul este zincat cu un strat de zinc pentru a-i oferi o rezistență mai mare la coroziune. În aceste procese, metalul care trebuie acoperit este utilizat ca anod, iar electrolitul este o sare solubilă a materialului anodic.
- Purificarea metalelor: poate fi aplicat și formulelor utilizate pentru rafinarea metalelor precum cuprul, zincul, staniu etc. De asemenea, prin proceduri de electroliză.
- Fabricarea produselor chimice: pentru a produce compuși chimici această constantă este de asemenea utilizată de obicei.
- Analiza chimica: prin electroliză s-ar putea determina și compoziția chimică.
- Producția de gaze: gaze precum oxigenul sau hidrogenul care sunt obținute din apă prin electroliză folosesc de asemenea această constantă pentru calcule.
- Medicină și esteticăElectroliza poate fi utilizată și pentru stimularea anumitor nervi sau tratarea anumitor probleme, pe lângă îndepărtarea părului nedorit. Fără constantă, nu ar fi putut fi dezvoltate o multitudine de instrumente de acest tip.
- Imprima: Pentru imprimante, procesele de electroliză sunt utilizate și pentru anumite elemente.
- Condensatoare electrolitice: o componentă electronică binecunoscută formată dintr-o peliculă subțire de oxid de aluminiu și un anod de aluminiu între electrozi. Electrolitul este un amestec de acid boric, glicerină și hidroxid de amoniu. Și așa se realizează acele mari capacități ...
Ce este electroliza?
Și întrucât constanta Faraday este atât de strâns legată de electrolizăSă vedem care este acest alt termen care este folosit foarte mult în industrie. Datorită acestui proces, elementele unui compus pot fi separate prin intermediul electricității. Acest lucru se face prin eliberarea de electroni de către anionii anodici (oxidare) și captarea electronilor de către cationii catodici (reducere).
A fost descoperit accidental de William Nicholson, în 1800, în timp ce studia funcționarea bateriilor chimice. În 1834, Michael Faraday a dezvoltat și publicat legile electrolizei.
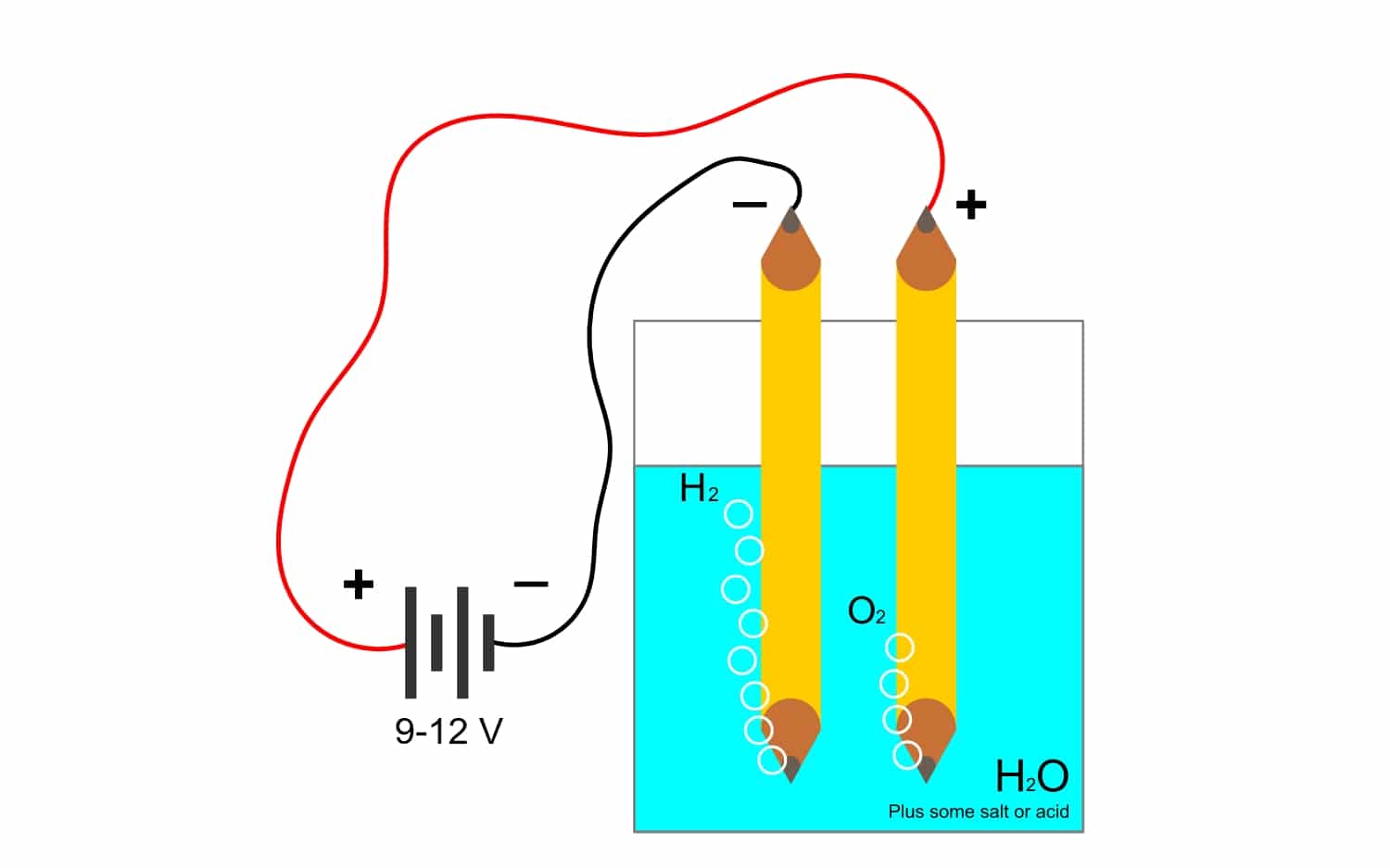
De exemplu, electroliza apă H2O, permite crearea de oxigen și hidrogen. Dacă se aplică un curent continuu prin electrozi, care vor separa oxigenul de hidrogen și vor putea izola ambele gaze (acestea nu pot intra în contact, deoarece produc o reacție explozivă foarte periculoasă).