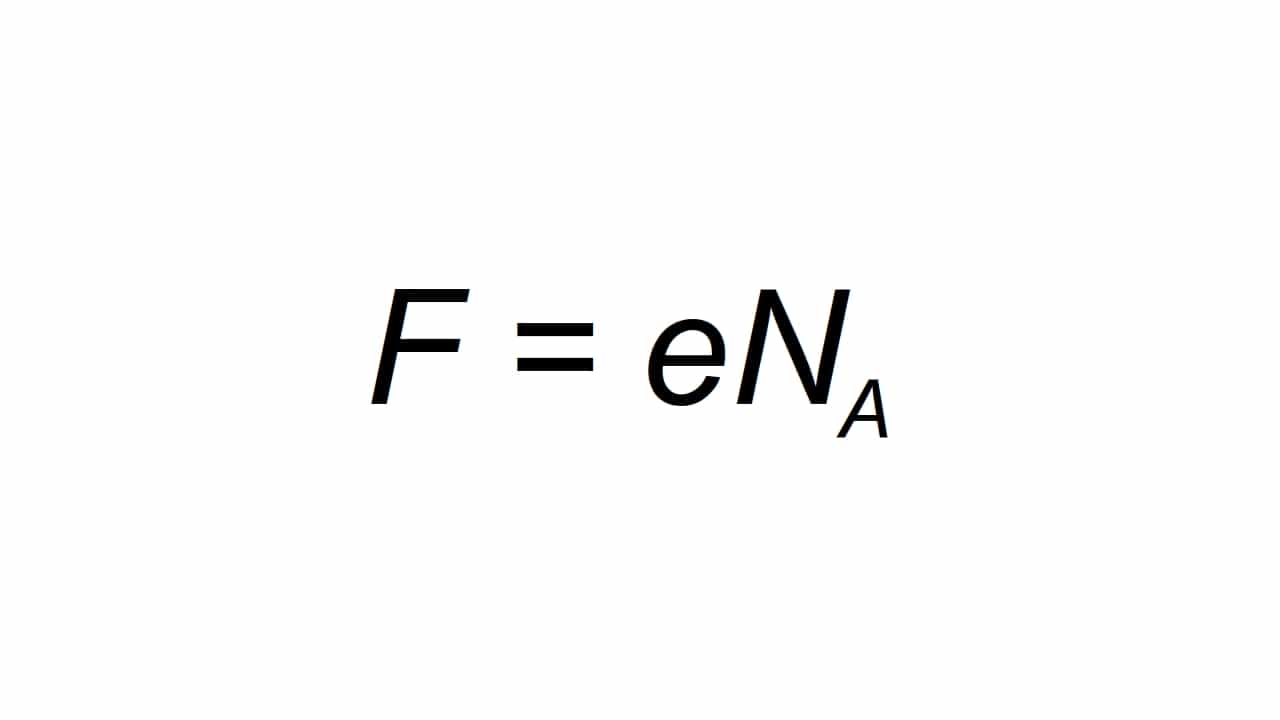Как и в другой раз, мы комментировали другие фундаментальные вопросы в области электроники и электричества, такие как Закон Омаили Законы Кирхгофа, и даже типы основных электрических цепей, также было бы интересно узнать, что это такое Постоянная Фарадея, так как это может помочь вам узнать немного больше о нагрузках.
В этой статье вы разберетесь немного лучше что такое постоянное блаженство, для чего он применяется и как рассчитывается ...
Что такое постоянная Фарадея?
La Постоянная Фарадея это постоянная, широко используемая в области физики и химии. Он определяется как количество электрического заряда на моль электронов. Его название происходит от британского ученого Майкла Фарадея. Эта константа может использоваться в электрохимических системах для расчета массы элементов, образующихся в электроде.
Его можно обозначить буквой F, и определяется как молярный элементарный заряд, способный подсчитывать как:
являющийся F итоговое значение постоянной Фарде, e - электрический заряд элемента, Na - постоянная Авогадро:
- е = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 моль-1
Согласно СИ эта постоянная Фарадея является точной, как и другие константы, и ее точное значение: 96485,3321233100184 Кл / моль. Как видите, он выражается в единицах Кл / моль, то есть кулонах на моль. И чтобы понять, что это за единицы, если вы еще не знаете, вы можете продолжить чтение следующих двух разделов ...
Что такое родинка?
Un моль единица измерения количества вещества. В системе СИ единиц это одна из 7 основных величин. В любом веществе, будь то элемент или химическое соединение, есть ряд элементарных единиц, составляющих его. Один моль будет эквивалентен 6,022 140 76 × 1023 элементарные сущности, представляющие собой фиксированное числовое значение константы Авогадро.
Эти элементарные объекты могут быть атомом, молекулой, ионом, электроном, фотонами или любым другим типом элементарной частицы. Например, с помощью этого вы можете рассчитать количество атомов что находится в грамме данного вещества.
En la химия, моль имеет фундаментальное значение, поскольку позволяет проводить множество расчетов составов, химических реакций и т. д. Например, для воды (H2О), у вас есть реакция 2 H2 + О2 → 2 часа2O, то есть два моля водорода (H2) и один моль кислорода (O2) реагируют с образованием двух молей воды. Кроме того, они также могут использоваться для выражения концентрации (см. Молярность).
Что такое электрический заряд?
С другой стороны, из электрический заряд Мы уже говорили о других случаях, это внутреннее физическое свойство некоторых субатомных частиц, которые проявляют силы притяжения и отталкивания между собой из-за электромагнитных полей. Электромагнитное взаимодействие между зарядом и электрическим полем является одним из 4 фундаментальных взаимодействий в физике, наряду с сильным ядерным взаимодействием, слабым ядерным взаимодействием и гравитационной силой.
Чтобы измерить этот электрический заряд, Кулон (C) или Кулон, и определяется как количество заряда, переносимого за одну секунду электрическим током силой один ампер.
Приложения постоянной Фарадея

Если вам интересно, что практическое применение У вас может быть эта постоянная Фарадея, правда в том, что у вас их довольно много, вот некоторые примеры:
- Гальваника / анодирование: для процессов в металлургической промышленности, где один металл покрывается другим путем электролиза. Например, когда сталь оцинкована слоем цинка, чтобы придать ей большую устойчивость к коррозии. В этих процессах покрываемый металл используется в качестве анода, а электролит представляет собой растворимую соль анодного материала.
- Очистка металлов: он также может применяться к формулам, используемым для очистки металлов, таких как медь, цинк, олово и т. д. Также с помощью процедур электролиза.
- Химическое производство: для образования химических соединений также обычно используется эта константа.
- Химический анализ: с помощью электролиза также может быть определен химический состав.
- Добыча газа: газы, такие как кислород или водород, полученные из воды путем электролиза, также используют эту константу для расчетов.
- Медицина и эстетикаЭлектролиз также можно использовать для стимуляции определенных нервов или лечения определенных проблем в дополнение к удалению нежелательных волос. Без константы невозможно было бы разработать множество инструментов этого типа.
- Печать: В принтерах для некоторых элементов также используются процессы электролиза.
- Электролитические конденсаторы: хорошо известный электронный компонент, состоящий из тонкой пленки оксида алюминия и алюминиевого анода между электродами. Электролит представляет собой смесь борной кислоты, глицерина и гидроксида аммония. И вот как достигаются эти великие способности ...
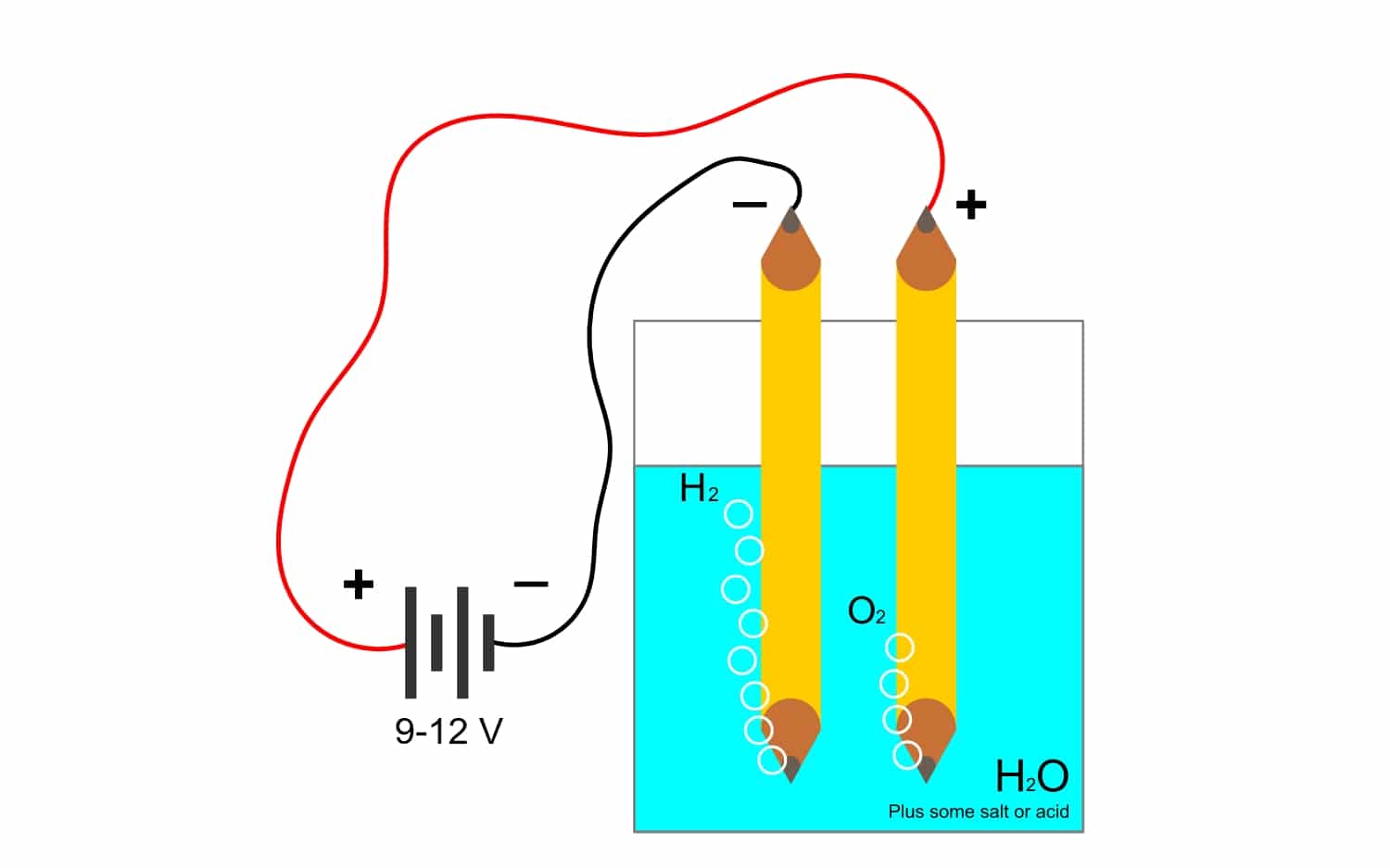
Что такое электролиз?
А поскольку постоянная Фарадея так тесно связана с электролизДавайте посмотрим, что это за другой термин, который часто используется в отрасли. Благодаря этому процессу элементы соединения можно разделить с помощью электричества. Это достигается за счет высвобождения электронов анодными анионами (окисление) и захвата электронов катодными катионами (восстановление).
Он был случайно обнаружен Уильямом Николсоном в 1800 году, изучая работу химических батарей. В 1834 г. Майкл Фарадей разработал и опубликовал законы электролиза.
Например, электролиз вода H2O, позволяет создавать кислород и водород. Если через электроды пропустить постоянный ток, который отделит кислород от водорода и сможет изолировать оба газа (они не могут вступить в контакт, поскольку вызывают очень опасную взрывную реакцию).