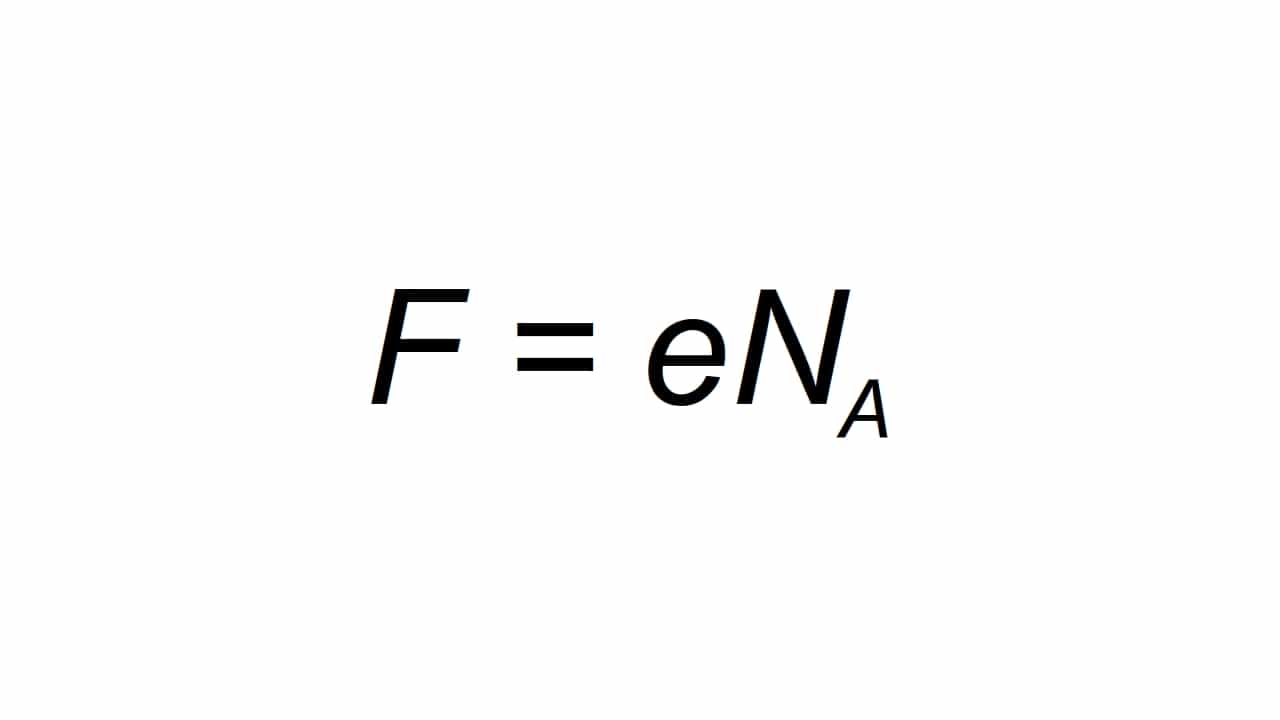Kot v drugih časih smo komentirali druga temeljna vprašanja s področja elektronike in električne energije, na primer Ohmov zakon, valovi Kirchoffovi zakoniin celo vrste osnovnih električnih vezij, zanimivo bi bilo tudi vedeti, kaj je to Faraday je stalnica, saj vam lahko pomaga vedeti malo več o obremenitvah.
V tem članku boste razumeli malo bolje kaj je stalna blaženost, za kaj se lahko prijavi in kako se izračuna ...
Kaj je Faradayjeva konstanta?
La Faraday je stalnica je stalnica, ki se pogosto uporablja na področjih fizike in kemije. Opredeljena je kot količina električnega naboja na mol elektronov. Njegovo ime izvira iz britanskega znanstvenika Michaela Faradaya. To konstanto lahko uporabimo v elektrokemičnih sistemih za izračun mase elementov, ki tvorijo elektrodo.
Lahko ga predstavimo s črko F, in je opredeljen kot molarni elementarni naboj, ki je sposoben izračunati kot:
Biti F nastala vrednost Fardayjeve konstante, e elementarnega električnega naboja, Na pa Avogadrova konstanta:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 mol-1
Po SI je ta Faradayeva konstanta natančna, tako kot druge konstante, njena natančna vrednost pa je: 96485,3321233100184 C / mol. Kot lahko vidite, je izražen v enoti C / mol, to je kuloni na mol. Če želite razumeti, kaj so te enote, če še ne veste, lahko nadaljujete z branjem naslednjih dveh razdelkov ...
Kaj je madež?
Un mol je enota, ki meri količino snovi. Znotraj SI enot je ena od 7 osnovnih količin. V kateri koli snovi, pa naj bo to element ali kemična spojina, obstaja vrsta elementarnih enot, ki jo sestavljajo. En mol bi bil enak 6,022 140 76 × 1023 osnovnih entitet, kar je fiksna numerična vrednost Avogadrove konstante.
Te elementarne entitete so lahko atom, molekula, ion, elektron, fotoni ali katera koli druga vrsta elementarnega delca. Na primer, s tem lahko izračunajte število atomov kaj je v gramu dane snovi.
V kemija, je mol bistven, saj omogoča številne izračune za sestave, kemijske reakcije itd. Na primer za vodo (H2O), imaš reakcijo 2 H2 + ALI2 → 2H2O, to je, da dva mola vodika (H2) in en mol kisika (O2) reagirajo in tvorijo dva mola vode. Poleg tega se lahko uporabljajo tudi za izražanje koncentracije (glej molarnost).
Kaj je električni naboj?
Po drugi strani pa iz električni naboj Govorili smo že ob drugih priložnostih, to je intrinzična fizikalna lastnost nekaterih subatomskih delcev, ki zaradi elektromagnetnih polj med njimi kažejo privlačne in odbojne sile. Elektromagnetna interakcija med nabojem in električnim poljem je ena od štirih temeljnih interakcij v fiziki, skupaj z močno jedrsko silo, šibko jedrsko silo in gravitacijsko silo.
Za merjenje tega električnega naboja je Coulomb (C) ali Coulomb, in je opredeljena kot količina naboja, ki jo v eni sekundi nosi električni tok z jakostjo enega ampera.
Aplikacije Faradayjeve konstante

Če se sprašujete, kaj praktična uporaba Lahko imaš to Faradayjevo konstanto, resnica je, da jih imaš kar nekaj, nekaj primerov je:
- Galvanizacija / eloksiranje: za procese v metalurški industriji, kjer se ena kovina prekrije z drugo z elektrolizo. Na primer, ko je jeklo pocinkano s plastjo cinka, da se poveča odpornost proti koroziji. Pri teh postopkih se kovina, ki jo je treba premazati, uporablja kot anoda, elektrolit pa je topna sol anodnega materiala.
- Čiščenje kovin: lahko se uporablja tudi za formule za rafiniranje kovin, kot so baker, cink, kositer itd. Tudi s postopki elektrolize.
- Kemična proizvodnja: za proizvodnjo kemičnih spojin se ta konstanta običajno uporablja tudi.
- Kemijska analiza: z elektrolizo bi lahko določili tudi kemično sestavo.
- Proizvodnja plina: plini, kot sta kisik ali vodik, pridobljeni iz vode z elektrolizo, prav tako uporabljajo to konstanto za izračune.
- Medicina in estetikaElektrolizo lahko poleg odstranjevanja neželenih dlak uporabimo tudi za stimulacijo določenih živcev ali zdravljenje določenih težav. Brez konstante ne bi bilo mogoče razviti množice tovrstnih orodij.
- Tiskanje: Za tiskalnike se za nekatere elemente uporabljajo tudi postopki elektrolize.
- Elektrolitski kondenzatorji: dobro znana elektronska komponenta, sestavljena iz tankega filma aluminijevega oksida in aluminijeve anode med elektrodama. Elektrolit je mešanica borove kisline, glicerina in amonijevega hidroksida. Tako se dosežejo te velike zmogljivosti ...
Kaj je elektroliza?
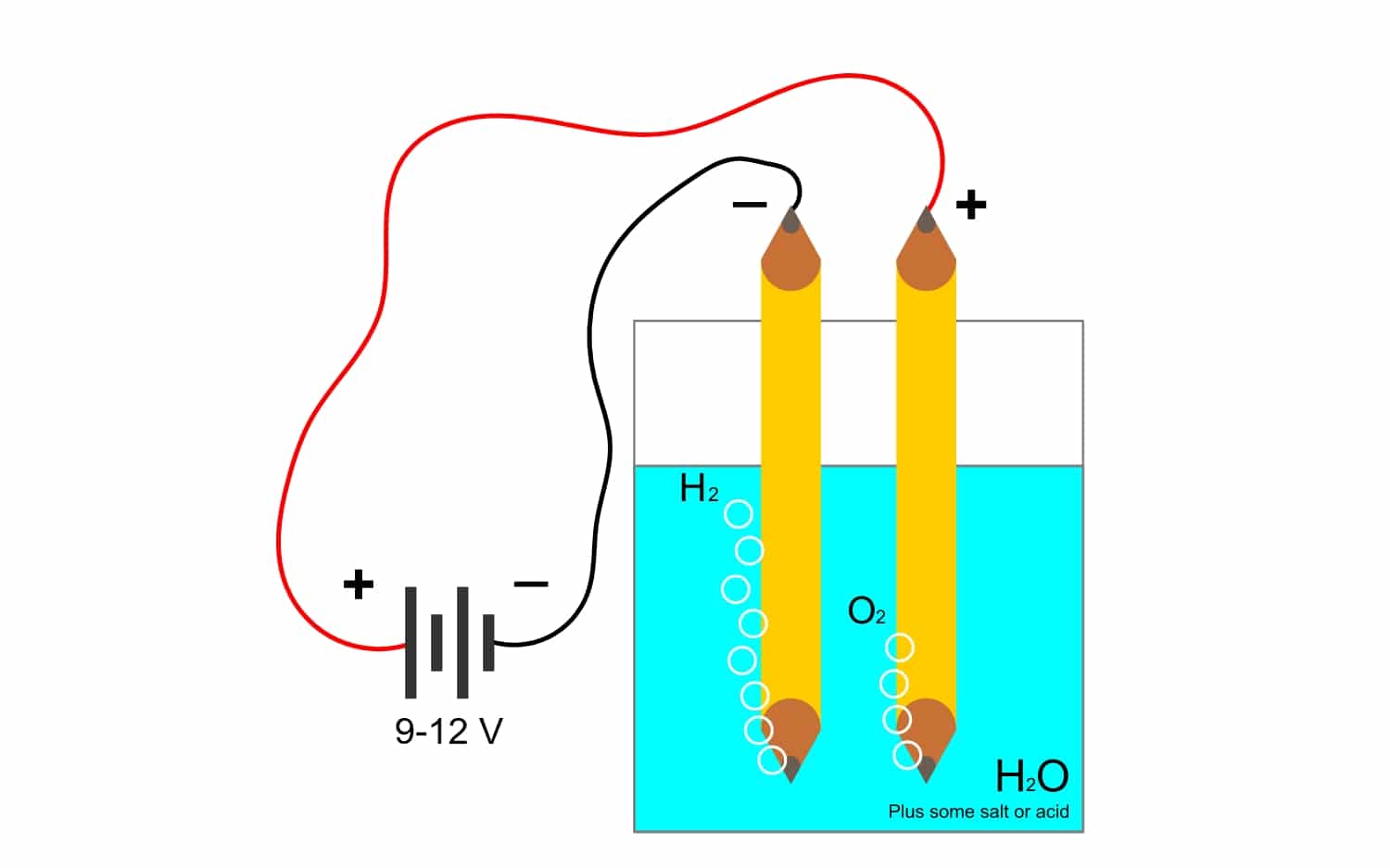
In ker je Faradayjeva konstanta tako tesno povezana z elektrolizaPoglejmo, kaj je ta drugi izraz, ki se v industriji pogosto uporablja. Zahvaljujoč temu postopku lahko elemente spojine ločimo s pomočjo električne energije. To dosežemo z sproščanjem elektronov z anodnimi anioni (oksidacija) in zajemanjem elektronov s katodnimi kationi (redukcija).
Po naključju ga je leta 1800 odkril William Nicholson, ko je preučeval delovanje kemičnih baterij. Leta 1834 je Michael faraday razvil in objavil zakone elektrolize.
Na primer elektroliza voda H2O, omogoča ustvarjanje kisika in vodika. Če skozi elektrode prihaja enosmerni tok, ki ločuje kisik od vodika in lahko izolira oba plina (ne moreta priti v stik, saj povzročata zelo nevarno eksplozivno reakcijo).