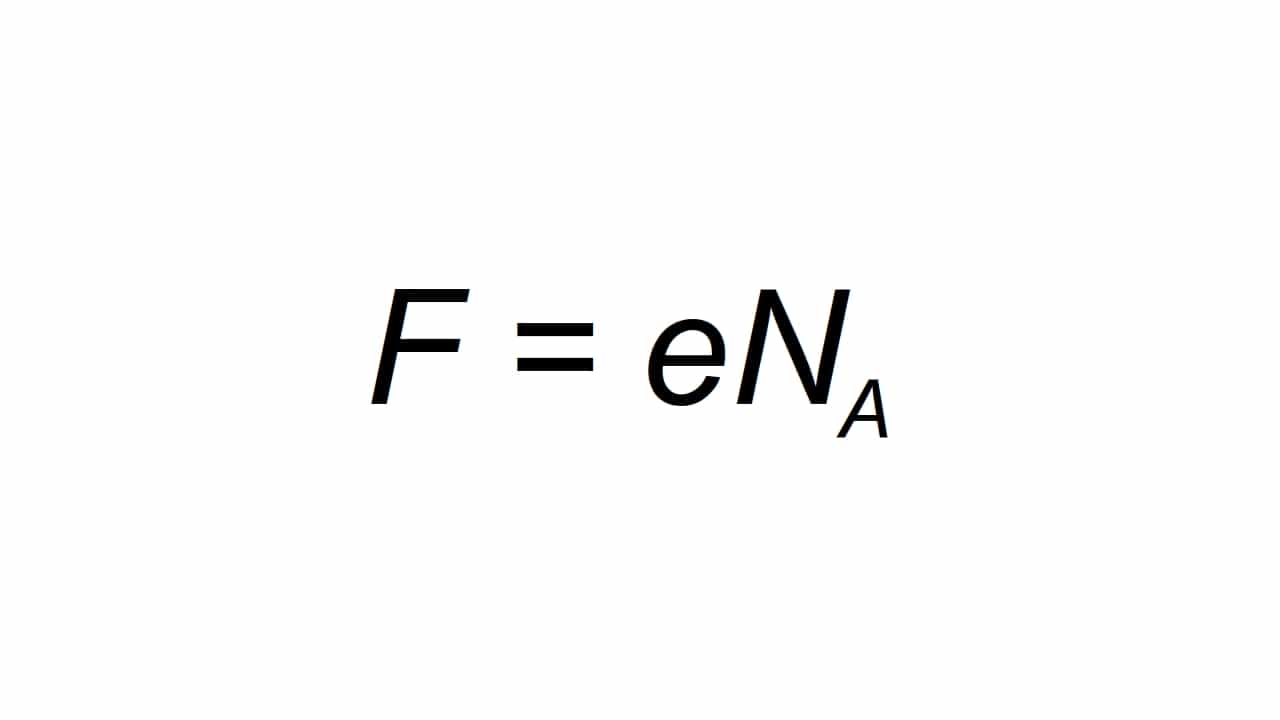மற்ற காலங்களைப் போலவே மின்னணு மற்றும் மின்சாரத் துறையில் உள்ள மற்ற அடிப்படை கேள்விகளுக்கு நாங்கள் கருத்து தெரிவித்துள்ளோம் ஓம் சட்டம், அலைகள் கிர்ச்சோப்பின் சட்டங்கள், மற்றும் கூட அடிப்படை மின்சுற்றுகளின் வகைகள்அது என்னவென்று தெரிந்துகொள்வதும் சுவாரஸ்யமாக இருக்கும் ஃபாரடேயின் மாறிலி, இது சுமைகளைப் பற்றி இன்னும் கொஞ்சம் தெரிந்து கொள்ள உதவும்.
இந்த கட்டுரையில் நீங்கள் கொஞ்சம் நன்றாக புரிந்துகொள்வீர்கள் நிலையான ஆனந்தம் என்றால் என்ன, எதற்கு விண்ணப்பிக்கலாம், எப்படி கணக்கிடப்படுகிறது ...
ஃபாரடே மாறிலி என்றால் என்ன?
La ஃபாரடேயின் மாறிலி இது தொடர்ந்து இயற்பியல் மற்றும் வேதியியல் துறைகளில் பரவலாக பயன்படுத்தப்படுகிறது. இது ஒரு மோல் எலக்ட்ரானுக்கு மின் கட்டணத்தின் அளவு என வரையறுக்கப்படுகிறது. இதன் பெயர் பிரிட்டிஷ் விஞ்ஞானி மைக்கேல் ஃபாரடேயிடமிருந்து வந்தது. எலக்ட்ரோடில் உருவாகும் தனிமங்களின் வெகுஜனத்தைக் கணக்கிட இந்த மாறிலி மின் வேதியியல் அமைப்புகளில் பயன்படுத்தப்படலாம்.
இது கடிதத்தால் குறிப்பிடப்படலாம் F, மற்றும் மோலார் அடிப்படை சார்ஜ் என வரையறுக்கப்படுகிறது கணக்கிட போன்ற:
இருப்பது F இதன் விளைவாக மதிப்பு ஃபார்டேயின் மாறிலி, மின் மின் கட்டணம், மற்றும் Na என்பது அவகாட்ரோவின் மாறிலி:
- e = 1.602176634 × 10-19 C
- நா = 6.02214076 × 1023 மோல்-1
SI இன் படி இந்த ஃபாரடே மாறிலி மற்ற மாறிலிகளைப் போல துல்லியமானது, அதன் துல்லியமான மதிப்பு: 96485,3321233100184 சி / மோல். நீங்கள் பார்க்க முடியும் என, இது அலகு C / mol இல் வெளிப்படுத்தப்படுகிறது, அதாவது, ஒரு மோலுக்கு கூலோம்ப்ஸ். இந்த அலகுகள் என்ன என்பதைப் புரிந்து கொள்ள, உங்களுக்கு இன்னும் தெரியாவிட்டால், அடுத்த இரண்டு பிரிவுகளை தொடர்ந்து படிக்கலாம் ...
மச்சம் என்றால் என்ன?
Un மோல் பொருளின் அளவை அளவிடும் அலகு ஆகும். அலகுகளின் SI க்குள், இது 7 அடிப்படை அளவுகளில் ஒன்றாகும். எந்தவொரு பொருளிலும், அது ஒரு உறுப்பு அல்லது இரசாயன கலவையாக இருந்தாலும், அதை உருவாக்கும் அடிப்படை அலகுகளின் தொடர் உள்ளது. ஒரு மோல் 6,022 140 76 × 10 க்கு சமமாக இருக்கும்23 அடிப்படை நிறுவனங்கள், இது அவகாட்ரோவின் மாறிலியின் நிலையான எண் மதிப்பு.
இந்த மூலக்கூறுகள் அணு, மூலக்கூறு, அயன், எலக்ட்ரான், ஃபோட்டான்கள் அல்லது வேறு எந்த அடிப்படைத் துகள்களாகவும் இருக்கலாம். உதாரணமாக, இதன் மூலம் உங்களால் முடியும் அணுக்களின் எண்ணிக்கையைக் கணக்கிடுங்கள் கொடுக்கப்பட்ட பொருளின் ஒரு கிராமில் என்ன இருக்கிறது.
இல் வேதியியல், மோல் அவசியம், ஏனெனில் இது கலவைகள், இரசாயன எதிர்வினைகள் போன்றவற்றுக்கு பல கணக்கீடுகளை செய்ய அனுமதிக்கிறது. உதாரணமாக, தண்ணீருக்கு (எச்2ஓ), உங்களுக்கு ஒரு எதிர்வினை உள்ளது 2 எச்2 + ஓ2 → 2 எச்2Oஅதாவது, இரண்டு மோல் ஹைட்ரஜன் (எச்2மற்றும் ஒரு ஆக்ஸிஜன் மோல் (ஓ2இரண்டு மோல் நீரை உருவாக்க வினைபுரிகிறது. மேலும், அவை செறிவை வெளிப்படுத்தவும் பயன்படுத்தப்படலாம் (மோலாரிட்டியைப் பார்க்கவும்).
மின் கட்டணம் என்றால் என்ன?
மறுபுறம், இருந்து மின்சார கட்டணம் நாங்கள் ஏற்கனவே மற்ற சந்தர்ப்பங்களில் பேசினோம், இது மின்காந்த புலங்கள் காரணமாக கவர்ச்சிகரமான மற்றும் விரட்டும் சக்திகளை வெளிப்படுத்தும் சில துணை அணு துகள்களின் உள்ளார்ந்த இயற்பியல் சொத்து. மின்சாரம் மற்றும் மின் புலத்திற்கு இடையிலான மின்காந்த தொடர்பு, வலுவான அணு சக்தி, பலவீனமான அணு சக்தி மற்றும் ஈர்ப்பு விசை ஆகியவற்றுடன் இயற்பியலில் உள்ள 4 அடிப்படை தொடர்புகளில் ஒன்றாகும்.
இந்த மின் கட்டணத்தை அளக்க, தி கூலம் (C) அல்லது கூலொம்ப், மற்றும் ஒரு ஆம்பியரின் தீவிரம் கொண்ட மின்னோட்டத்தால் ஒரு வினாடியில் கொண்டு செல்லப்படும் கட்டணத்தின் அளவு என வரையறுக்கப்படுகிறது.
ஃபாரடே மாறிலியின் பயன்பாடுகள்

என்ன என்று ஆச்சரியப்பட்டால் நடைமுறை பயன்பாடு நீங்கள் இந்த ஃபாரடே மாறிலி வைத்திருக்கலாம், உண்மை என்னவென்றால், உங்களிடம் சில உள்ளன, சில உதாரணங்கள்:
- எலக்ட்ரோபிளேட்டிங் / அனோடைசிங்: உலோகவியல் தொழிற்துறையில் உள்ள செயல்முறைகளுக்கு ஒரு உலோகம் மற்றொன்றால் மின்னாற்பகுப்பு மூலம் மூடப்பட்டிருக்கும். உதாரணமாக, துத்தநாக அடுக்குடன் எஃகு கால்வனைஸ் செய்யப்படும்போது அது அரிப்புக்கு அதிக எதிர்ப்பைக் கொடுக்கும். இந்த செயல்முறைகளில், பூசப்பட வேண்டிய உலோகம் ஆனோடாகப் பயன்படுத்தப்படுகிறது மற்றும் எலக்ட்ரோலைட் ஆனோட் பொருளின் கரையக்கூடிய உப்பாகும்.
- உலோக சுத்திகரிப்பு: செம்பு, துத்தநாகம், தகரம் போன்ற உலோகங்களின் சுத்திகரிப்புக்காக பயன்படுத்தப்படும் சூத்திரங்களுக்கும் இதைப் பயன்படுத்தலாம். மேலும் மின்னாற்பகுப்பு நடைமுறைகள் மூலம்.
- இரசாயன உற்பத்தி: இரசாயன கலவைகளை உற்பத்தி செய்ய இந்த மாறிலி பொதுவாக பயன்படுத்தப்படுகிறது.
- இரசாயன பகுப்பாய்வு: மின்னாற்பகுப்பு மூலம் வேதியியல் கலவையையும் தீர்மானிக்க முடியும்.
- எரிவாயு உற்பத்தி: மின்னாற்பகுப்பு மூலம் நீரிலிருந்து பெறப்படும் ஆக்ஸிஜன் அல்லது ஹைட்ரஜன் போன்ற வாயுக்களும் கணக்கீடுகளுக்கு இந்த மாறிலியைப் பயன்படுத்துகின்றன.
- மருத்துவம் மற்றும் அழகியல்மின்னாற்பகுப்பு தேவையற்ற முடிகளை அகற்றுவதோடு, சில நரம்புகளைத் தூண்டவும் அல்லது சில பிரச்சனைகளுக்கு சிகிச்சையளிக்கவும் பயன்படுகிறது. கான்ஸ்டன்ட் இல்லாமல், இந்த வகை கருவிகளை உருவாக்கியிருக்க முடியாது.
- அச்சிடும் சேவைகள்அச்சுப்பொறிகளுக்கு, மின்னாற்பகுப்பு செயல்முறைகள் சில உறுப்புகளுக்கும் பயன்படுத்தப்படுகின்றன.
- மின்னாற்பகுப்பு மின்தேக்கிகள்: அலுமினிய ஆக்சைடு மெல்லிய படலம் மற்றும் மின்முனைகளுக்கு இடையில் ஒரு அலுமினியம் அனோட் கொண்ட நன்கு அறியப்பட்ட மின்னணு கூறு. எலக்ட்ரோலைட் என்பது போரிக் அமிலம், கிளிசரின் மற்றும் அம்மோனியம் ஹைட்ராக்சைடு ஆகியவற்றின் கலவையாகும். இந்த பெரிய திறன்கள் எவ்வாறு அடையப்படுகின்றன ...
மின்னாற்பகுப்பு என்றால் என்ன?
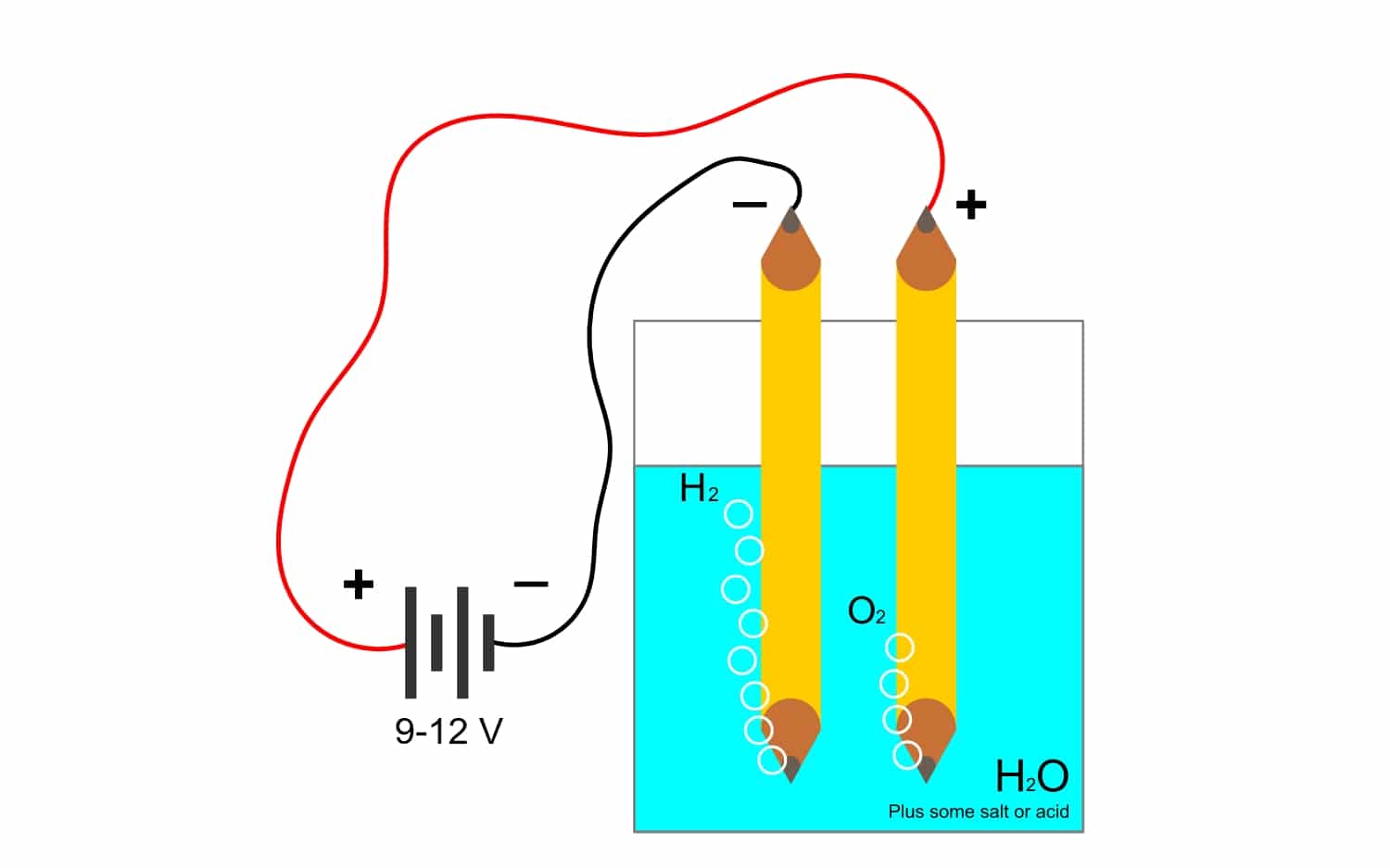
மேலும் ஃபாரடே கான்ஸ்டன்ட் மிகவும் நெருக்கமாக தொடர்புடையது மின்னாற்பகுப்புதொழிலில் அதிகம் பயன்படுத்தப்படும் இந்த வேறு சொல் என்ன என்பதைப் பார்ப்போம். இந்த செயல்முறைக்கு நன்றி, ஒரு கலவையின் கூறுகளை மின்சாரம் மூலம் பிரிக்கலாம். அனோட் அனான்கள் (ஆக்ஸிஜனேற்றம்) மூலம் எலக்ட்ரான்களை வெளியிடுவதன் மூலமும், கேத்தோடு கேஷன்களால் (குறைத்தல்) எலக்ட்ரான்களைப் பிடிப்பதன் மூலமும் இது செய்யப்படுகிறது.
1800 ஆம் ஆண்டில், ரசாயன பேட்டரிகளின் செயல்பாட்டைப் படிக்கும் போது, தற்செயலாக வில்லியம் நிக்கல்சன் கண்டுபிடித்தார். 1834 இல், மைக்கேல் ஃபாரடே மின்னாற்பகுப்பு விதிகளை உருவாக்கி வெளியிட்டார்.
உதாரணமாக, மின்னாற்பகுப்பு நீர் எச்2O, ஆக்ஸிஜன் மற்றும் ஹைட்ரஜனை உருவாக்க அனுமதிக்கிறது. ஹைட்ரஜனிலிருந்து ஆக்ஸிஜனைப் பிரித்து, இரண்டு வாயுக்களையும் தனிமைப்படுத்தக்கூடிய மின்முனைகள் மூலம் நேரடி மின்னோட்டம் பயன்படுத்தப்பட்டால் (அவை மிகவும் ஆபத்தான வெடிக்கும் எதிர்வினையை உருவாக்கும் என்பதால் அவை தொடர்பு கொள்ள முடியாது).