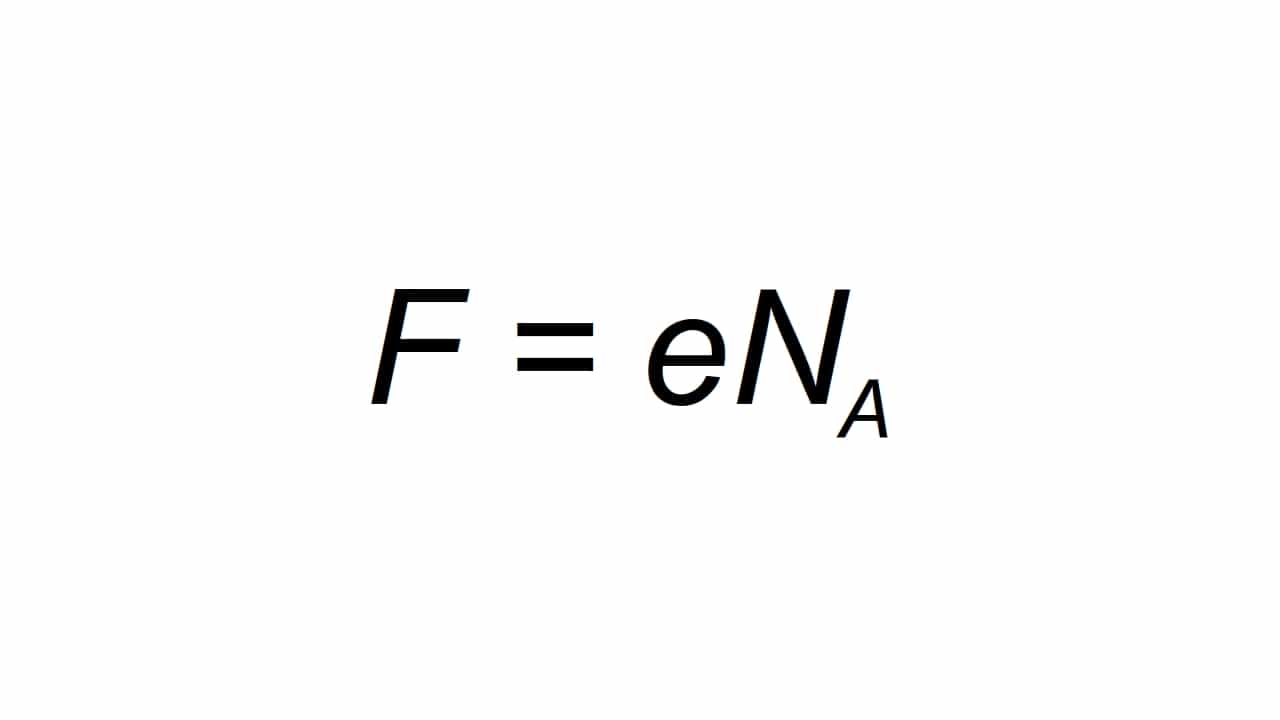Diğer zamanlarda olduğu gibi, elektronik ve elektrik alanındaki diğer temel sorular hakkında yorum yaptık, örneğin: Ohm kanunu, dalgalar Kirchoff yasalarıve hatta temel elektrik devreleri türleri, ne olduğunu bilmek de ilginç olurdu Faraday sabiti, yükler hakkında biraz daha fazla bilgi sahibi olmanıza yardımcı olabileceğinden.
Bu yazıda biraz daha iyi anlayacaksınız sürekli mutluluk nedir, ne için başvurulabilir, nasıl hesaplanır...
Faraday sabiti nedir?
La Faraday sabiti fizik ve kimya alanlarında yaygın olarak kullanılan bir sabittir. Elektron molü başına elektrik yükü miktarı olarak tanımlanır. Adı İngiliz bilim adamı Michael Faraday'dan geliyor. Bu sabit, bir elektrotta oluşan elementlerin kütlesini hesaplamak için elektrokimyasal sistemlerde kullanılabilir.
Harf ile temsil edilebilir. F, ve mümkün olmak, molar elemental yük olarak tanımlanır hesaplamak gibi:
varlık F sonuçtaki değer Farday sabiti, e temel elektrik yükü ve Na, Avogadro sabitidir:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 köstebek-1
SI'ye göre, bu Faraday sabiti, diğer sabitler gibi kesindir ve kesin değeri: 96485,3321233100184C/mol. Gördüğünüz gibi, C / mol biriminde, yani mol başına coulomb cinsinden ifade edilir. Ve bu birimlerin ne olduğunu anlamak için henüz bilmiyorsanız sonraki iki bölümü okumaya devam edebilirsiniz...
Köstebek nedir?
Un köstebek madde miktarını ölçen bir birimdir. Birimlerin SI içinde, 7 temel miktardan biridir. Herhangi bir maddede, ister element ister kimyasal bileşik olsun, onu oluşturan bir dizi temel birim vardır. Bir mol, 6,022 140 76 × 10'a eşittir23 Avogadro sabitinin sabit sayısal değeri olan temel varlıklar.
Bu temel varlıklar bir atom, bir molekül, bir iyon, bir elektron, fotonlar veya başka herhangi bir temel parçacık türü olabilir. Örneğin, bununla yapabilirsiniz atom sayısını hesapla Belirli bir maddenin bir gramında ne var?
In kimya, köstebek esastır, çünkü bileşimler, kimyasal reaksiyonlar vb. için birçok hesaplamanın yapılmasına izin verir. Örneğin, su için (H2O), bir tepkin var 2 H2 + O2 → 2 Saat2Oyani iki mol hidrojen (H2) ve bir mol oksijen (O2) reaksiyona girerek iki mol su oluşturur. Ayrıca, konsantrasyonu ifade etmek için de kullanılabilirler (bkz. molarite).
Elektrik yükü nedir?
Öte yandan, elektrik şarjı Daha önce başka vesilelerle konuştuk, elektromanyetik alanlar nedeniyle aralarında çekici ve itici güçler gösteren bazı atom altı parçacıkların içsel bir fiziksel özelliğidir. Yük ve elektrik alanı arasındaki elektromanyetik etkileşim, güçlü nükleer kuvvet, zayıf nükleer kuvvet ve yerçekimi kuvveti ile birlikte fizikteki 4 temel etkileşimden biridir.
Bu elektrik yükünü ölçmek için, Coulomb (C) veya Coulomb, ve şiddeti bir amper olan bir elektrik akımının bir saniyede taşıdığı yük miktarı olarak tanımlanır.
Faraday sabitinin uygulamaları

Ne olduğunu merak ediyorsan pratik uygulama Bu Faraday sabitine sahip olabilirsiniz, gerçek şu ki elinizde epeyce var, bazı örnekler:
- Galvanik / eloksal: metalurji endüstrisinde, bir metalin elektroliz yoluyla başka bir metalle kaplandığı prosesler için. Örneğin, çelik, korozyona karşı daha fazla direnç sağlamak için bir çinko tabakasıyla galvanizlendiğinde. Bu işlemlerde kaplanacak metal anot olarak kullanılır ve elektrolit anot malzemesinin çözünür bir tuzudur.
- Metal arıtma: Bakır, çinko, kalay vb. metallerin arıtılmasında kullanılan formüllere de uygulanabilir. Ayrıca elektroliz prosedürleri ile.
- Kimyasal üretim: kimyasal bileşikler üretmek için bu sabit de genellikle kullanılır.
- Kimyasal analiz: elektroliz ile kimyasal bileşim de belirlenebilir.
- Gaz üretimi: Elektroliz yoluyla sudan elde edilen oksijen veya hidrojen gibi gazlar da bu sabiti hesaplamalar için kullanır.
- Tıp ve estetikElektroliz, istenmeyen tüyleri almanın yanı sıra belirli sinirleri uyarmak veya belirli sorunları tedavi etmek için de kullanılabilir. Sabit olmadan, bu türden çok sayıda araç geliştirilemezdi.
- Impresión: Yazıcılarda belirli elemanlar için elektroliz işlemleri de kullanılmaktadır.
- Elektrolitik kapasitörler: ince bir alüminyum oksit filminden ve elektrotlar arasında bir alüminyum anottan oluşan iyi bilinen bir elektronik bileşen. Elektrolit, borik asit, gliserin ve amonyum hidroksitin bir karışımıdır. İşte bu büyük kapasiteler böyle elde edilir...
elektroliz nedir?
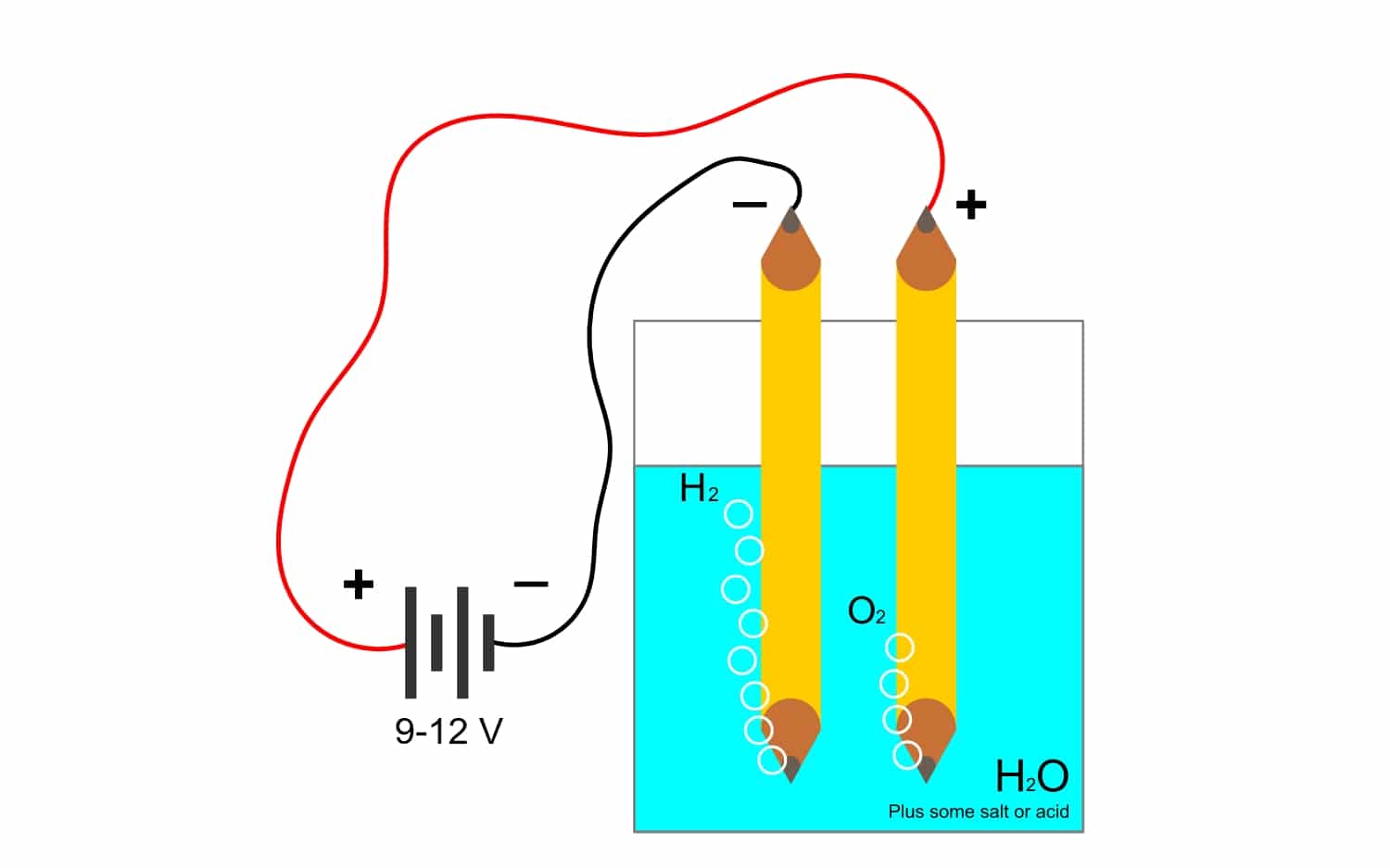
Faraday sabiti ile çok yakından ilişkili olduğu için elektrolizBakalım sektörde çokça kullanılan bu diğer terim neymiş. Bu işlem sayesinde bir bileşiğin elementleri elektrik yoluyla ayrılabilir. Bu, elektronların anot anyonları tarafından salınması (oksidasyon) ve elektronların katot katyonları tarafından yakalanması (indirgenme) ile yapılır.
William Nicholson tarafından 1800 yılında kimyasal pillerin işleyişini incelerken tesadüfen keşfedildi. 1834 yılında Michael Faraday elektroliz yasalarını geliştirdi ve yayınladı.
Örneğin, elektroliz su H2O, oksijen ve hidrojen oluşturmasını sağlar. Elektrotlar aracılığıyla oksijeni hidrojenden ayıracak ve her iki gazı da izole edebilecek bir doğru akım uygulanırsa (çok tehlikeli bir patlayıcı reaksiyon ürettikleri için temas edemezler).