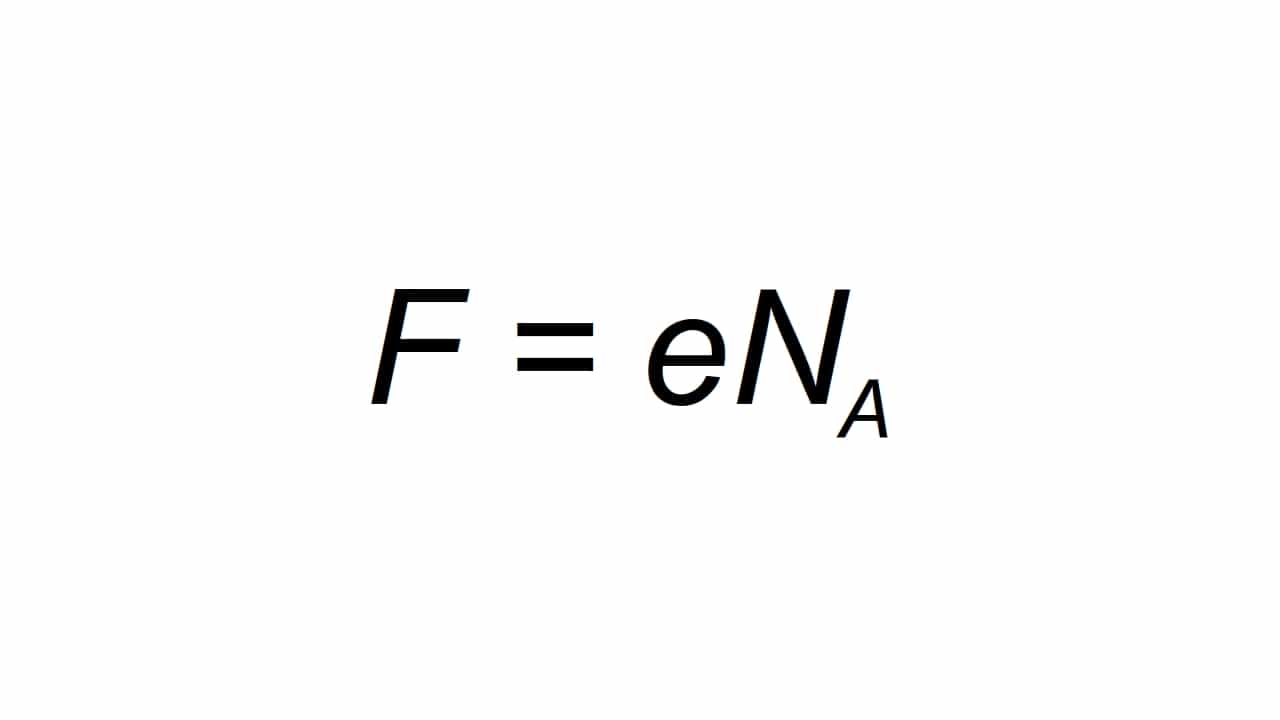Як і інший раз, ми коментували інші фундаментальні питання в галузі електроніки та електрики, такі як Закон Ома, хвилі Закони Кірхофаі навіть типи основних електричних ланцюгів, також було б цікаво дізнатися, що це таке Постійна Фарадея, оскільки це може допомогти вам дізнатися трохи більше про навантаження.
У цій статті ви трохи краще зрозумієте що таке постійне щастя, на що його можна подати, і як його розрахувати ...
Що таке константа Фарадея?
La Постійна Фарадея це константа, яка широко використовується у галузях фізики та хімії. Він визначається як кількість електричного заряду на моль електронів. Його назва походить від британського вченого Майкла Фарадея. Ця константа може бути використана в електрохімічних системах для розрахунку маси елементів, які утворюються в електроді.
Його можна зобразити літерою F, і визначається як молярний елементний заряд, здатний розрахувати як:
Буття F отримане значення постійної Фардея, e елементарного електричного заряду, а Na - постійної Авогадро:
- e = 1.602176634 × 10-19 C
- Na = 6.02214076 × 1023 М-1
Відповідно до СІ, ця константа Фарадея точна, як і інші константи, і її точне значення дорівнює: 96485,3321233100184 С / моль. Як бачите, вона виражена в одиниці С / моль, тобто кулонів на моль. І щоб зрозуміти, що це за одиниці, якщо ви ще не знаєте, ви можете продовжити читати наступні два розділи ...
Що таке родимка?
Un М - це одиниця вимірювання кількості речовини. У межах СІ одиниць це одна з 7 фундаментальних величин. У будь -якій речовині, будь то елемент або хімічна сполука, існує ряд елементарних одиниць, які її складають. Один моль еквівалентний 6,022 140 76 × 1023 елементарних сутностей, що є фіксованим числовим значенням постійної Авогадро.
Ці елементарні сутності можуть бути атомом, молекулою, іоном, електроном, фотонами або будь -яким іншим типом елементарних частинок. Наприклад, з цим можна обчислити кількість атомів що міститься у грамі даної речовини.
В хімія, моль є фундаментальним, оскільки дозволяє проводити багато розрахунків щодо складів, хімічних реакцій тощо. Наприклад, для води (H2О), у вас є реакція 2 H2 + O2 → 2 год2O, тобто два молі водню (H2) і один моль кисню (O2) реагують, утворюючи два молі води. Крім того, вони також можуть бути використані для вираження концентрації (див. Молярність).
Що таке електричний заряд?
З іншого боку, від електричний заряд Ми вже говорили в інших випадках, це внутрішня фізична властивість деяких субатомних частинок, які проявляють привабливі та відштовхувальні сили між ними через електромагнітні поля. Електромагнітна взаємодія між зарядом та електричним полем є однією з 4 фундаментальних взаємодій у фізиці разом із сильною ядерною силою, слабкою ядерною силою та силою тяжіння.
Щоб виміряти цей електричний заряд, Кулон (С) або Кулон, і визначається як кількість заряду, що переноситься за одну секунду електричним струмом інтенсивністю один ампер.
Застосування константи Фарадея

Якщо вам цікаво, що практичне застосування Ви можете мати цю постійну Фарадея, правда в тому, що у вас їх досить багато, деякі приклади:
- Гальваніка / анодування: для процесів у металургійній промисловості, де один метал покривається іншим електролізом. Наприклад, коли сталь оцинкована шаром цинку, щоб надати їй більшу стійкість до корозії. У цих процесах метал, що покривається, використовується як анод, а електроліт - це розчинна сіль анодного матеріалу.
- Очищення металу: він також може бути застосований до формул, що використовуються для очищення металів, таких як мідь, цинк, олово тощо. Також методами електролізу.
- Хімічне виробництво: для отримання хімічних сполук цю константу також зазвичай використовують.
- Хімічний аналіз: шляхом електролізу можна також визначити хімічний склад.
- Видобуток газу: такі гази, як кисень або водень, отримані з води електролізом, також використовують цю константу для розрахунків.
- Медицина та естетикаЕлектроліз також може бути використаний для стимуляції певних нервів або лікування певних проблем, на додаток до видалення небажаного волосся. Без константи не могло б бути розроблено безліч інструментів такого типу.
- Друк: Для принтерів також використовують процеси електролізу для певних елементів.
- Електролітичні конденсатори: відомий електронний компонент, що складається з тонкої плівки оксиду алюмінію та алюмінієвого аноду між електродами. Електроліт являє собою суміш борної кислоти, гліцерину та гідроксиду амонію. Ось як досягаються ці великі можливості ...
Що таке електроліз?
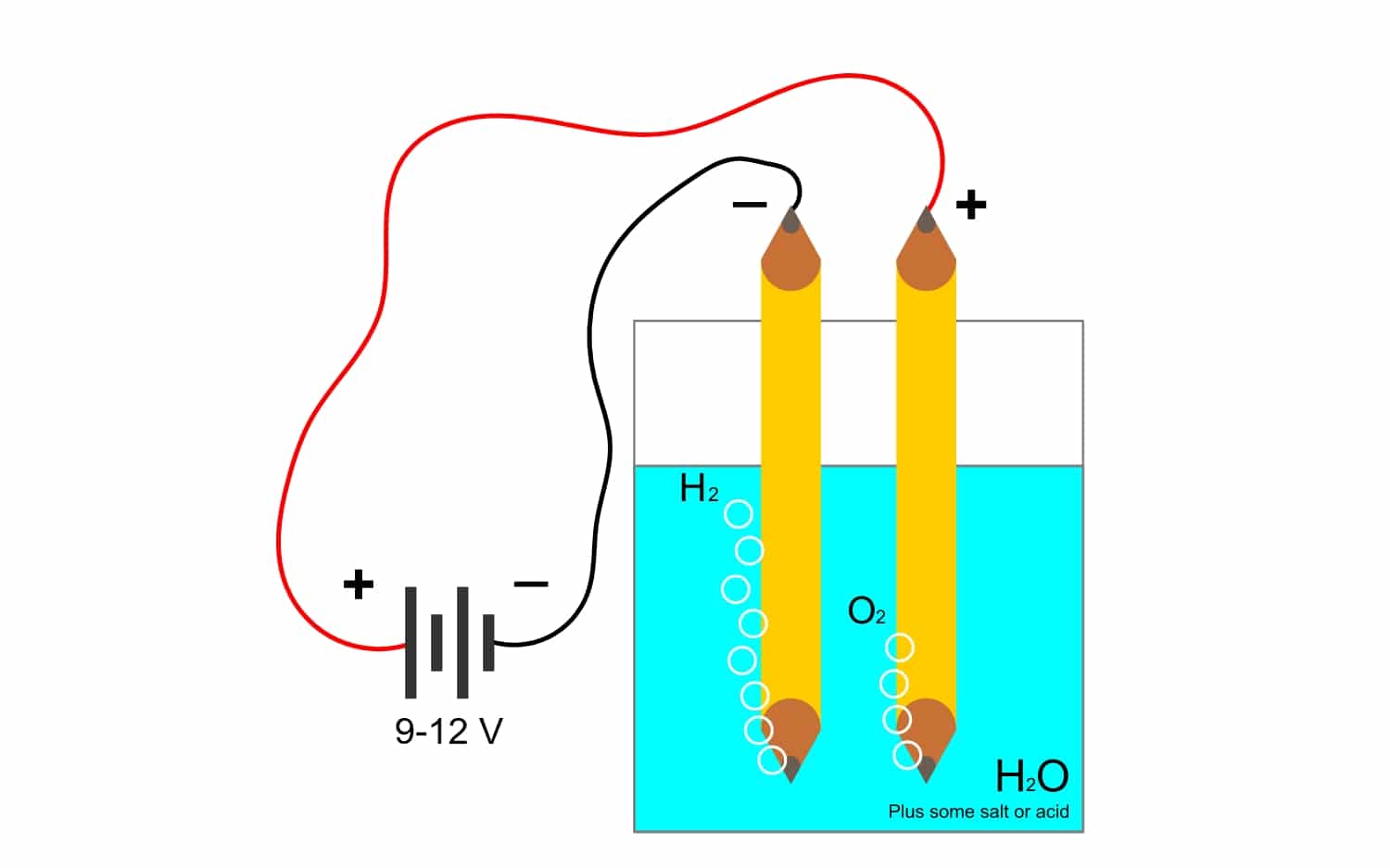
А оскільки константа Фарадея настільки тісно пов'язана з електролізДавайте подивимося, що це за інший термін, який багато використовується в промисловості. Завдяки цьому процесу елементи з'єднання можна відокремити за допомогою електрики. Це відбувається шляхом вивільнення електронів анодними аніонами (окислення) та захопленням електронів катодними катіонами (відновлення).
Він був випадково відкритий Вільямом Ніколсоном у 1800 році під час вивчення роботи хімічних батарей. У 1834 р. Майкл Фарадей розробив і опублікував закони електролізу.
Наприклад, електроліз вода Н2O, дозволяє створювати кисень і водень. Якщо через електроди подавати постійний струм, який відокремлює кисень від водню і здатний ізолювати обидва гази (вони не можуть контактувати, оскільки вони викликають дуже небезпечну вибухову реакцію).