
Al igual que otras veces hemos comentado sobre otras cuestiones fundamentales en el campo de la electrónica y la electricidad, como la ley de Ohm, o las leyes de Kirchoff, e incluso los tipos de circuitos eléctricos básicos, también sería interesante conocer qué es la constante de Faraday, ya que te puede ayudar a saber un poco más de las cargas.
En este artículo podrás comprender un poco mejor qué es dicha constante, para qué se puede aplicar, y cómo se calcula…
¿Qué es la constante de Faraday?

La constante de Faraday es una constante muy empleada en los campos de la física y la química. Se define como la cantidad de carga eléctrica por mol de electrones. Su nombre proviene en honor al científico británico Michael Faraday. Esta constante se puede usar en los sistemas electroquímicos para calcular la masa de los elementos que se forman en un electrodo.
Se puede representar por la letra F, y se define como la carga elemental molar, pudiéndose calcular como:
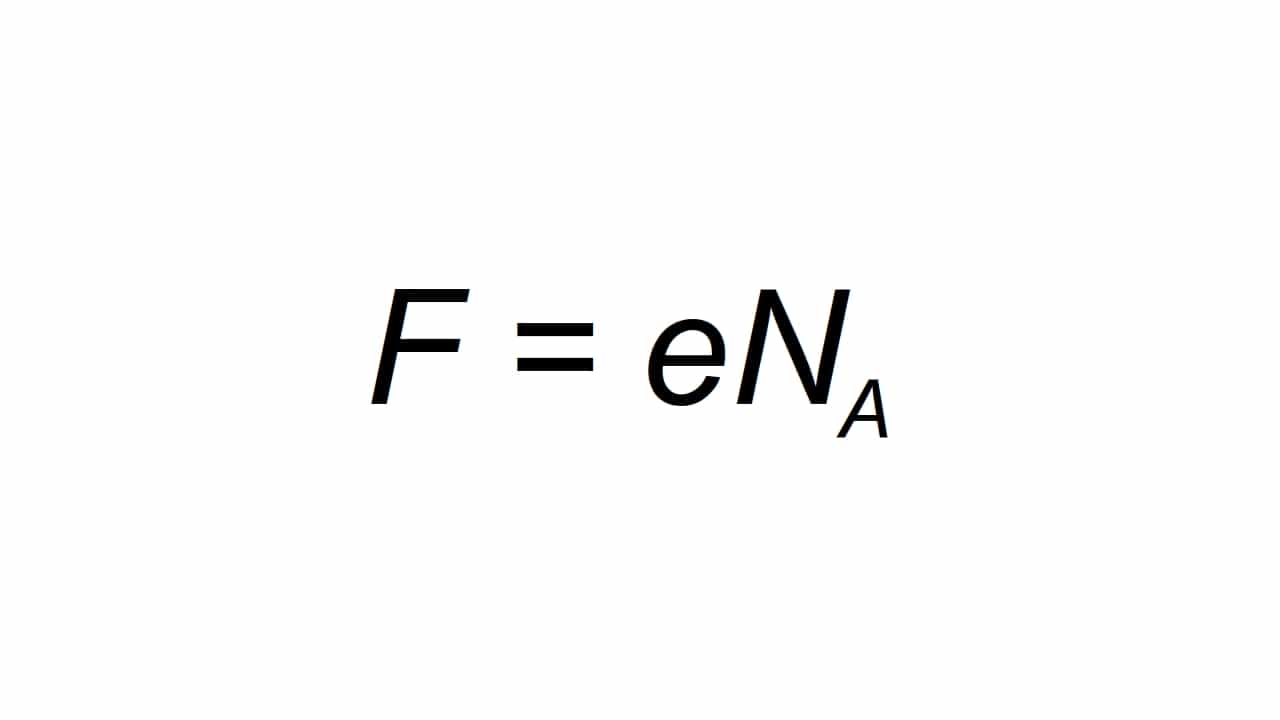
Siendo F el valor resultante de la constante de Farday, e la carga eléctrica elemental, y Na la constante de Avogadro:
- e = 1.602176634×10-19 C
- Na = 6.02214076×1023 mol-1
Según el S.I. esta constante de Faraday es exacta, al igual que otras constantes, y su valor preciso es de: 96485,3321233100184 C/mol. Como puedes ver, se expresa en la unidad C/mol, es decir, culombios por mol. Y para entender qué son estas unidades, si no lo sabes aún, puedes seguir leyendo los dos siguientes apartados…
¿Qué es un mol?
Un mol es una unidad que mide la cantidad de sustancia. Dentro del S.I. de unidades, es una de las 7 magnitudes fundamentales. En cualquier sustancia, ya sea un elemento o un compuesto químico, hay una serie de unidades elementales que lo componen. Un mol sería equivalente a 6,022 140 76 × 1023 entidades elementales, que es el valor numérico fijo de la constante de Avogadro.
Estas entidades elementales pueden ser un átomo, una molécula, un ión, un electrón, fotones, o cualquier otro tipo de partícula elemental. Por ejemplo, con ello se pueden calcular la cantidad de átomos que hay en un gramo de una sustancia dada.
En la química, el mol es fundamental, ya que permite hacer muchos cálculos para las composiciones, reacciones químicas, etc. Por ejemplo, para el agua (H2O), se tiene una reacción 2 H2 + O2 → 2 H2O, es decir, que dos moles de hidrógeno (H2) y un mol de oxígeno (O2) reaccionan para formar dos moles de agua. Además, también se pueden usar para expresar la concentración (véase molaridad).
¿Qué es la carga eléctrica?
Por otro lado, de la carga eléctrica ya hemos hablado en otras ocasiones, se trata de una propiedad física intrínseca de algunas partículas subatómicas que manifiestan fuerzas de atracción y repulsión entre ellas debido a unos campos electromagnéticos. La interacción electromagnética, entre la carga y el campo eléctrico, es una de las 4 interacciones fundamentales de la física, junto con la fuerza nuclear fuerte, fuerza nuclear débil, y la gravitatoria.
Para medir esta carga eléctrica se emplea el Coulomb (C) o Culombio, y está definida como la cantidad de carga transportada en un segundo por una corriente eléctrica de un amperio de intensidad.
Aplicaciones de la constante de Faraday

Si te preguntas qué aplicación práctica puede tener esta constante de Faraday, la verdad es que tiene bastantes, algunos ejemplos son:
- Galvanoplastia/anodización: para los procesos de la industria metalúrgica donde un metal se recubre de otro mediante electrólisis. Por ejemplo, cuando el acero se galvaniza con una capa de zinc para darle mayor resistencia a la corrosión. En estos procesos se emplea el metal a recubrir como ánodo y el electrolito es una sal soluble del material del ánodo.
- Purificación de metales: también se puede aplicar a las fórmulas empleadas para el refinamiento de metales como el cobre, zinc, estaño, etc. También por procedimientos de electrólisis.
- Fabricación de químicos: para producir compuestos químicos también se suele emplear esta constante.
- Análisis químico: mediante electrólisis también se podría determinar la composición química.
- Producción de gases: gases como el oxígeno o el hidrógeno que se obtienen a partir del agua mediante electrólisis también usan esta constante para los cálculos.
- Medicina y estética: también se pueden usar electrólisis para estimular ciertos nervios o tratar ciertos problemas, además de eliminar el vello no deseado. Sin la constante, no se podrían haber desarrollado multitud de herramientas de este tipo.
- Impresión: para las imprentas también se emplean procesos de electrólisis para ciertos elementos.
- Condensadores electrolíticos: un componente electrónico muy conocido y que se compone de una película delgada de óxido de aluminio y un ánodo de aluminio entre electrodos. El electrolito es una mezcla de ácido bórico, gilcerina e hidróxido de amonio. Y así es como se consiguen esas capacidades tan grandes…
¿Qué es la electrólisis?
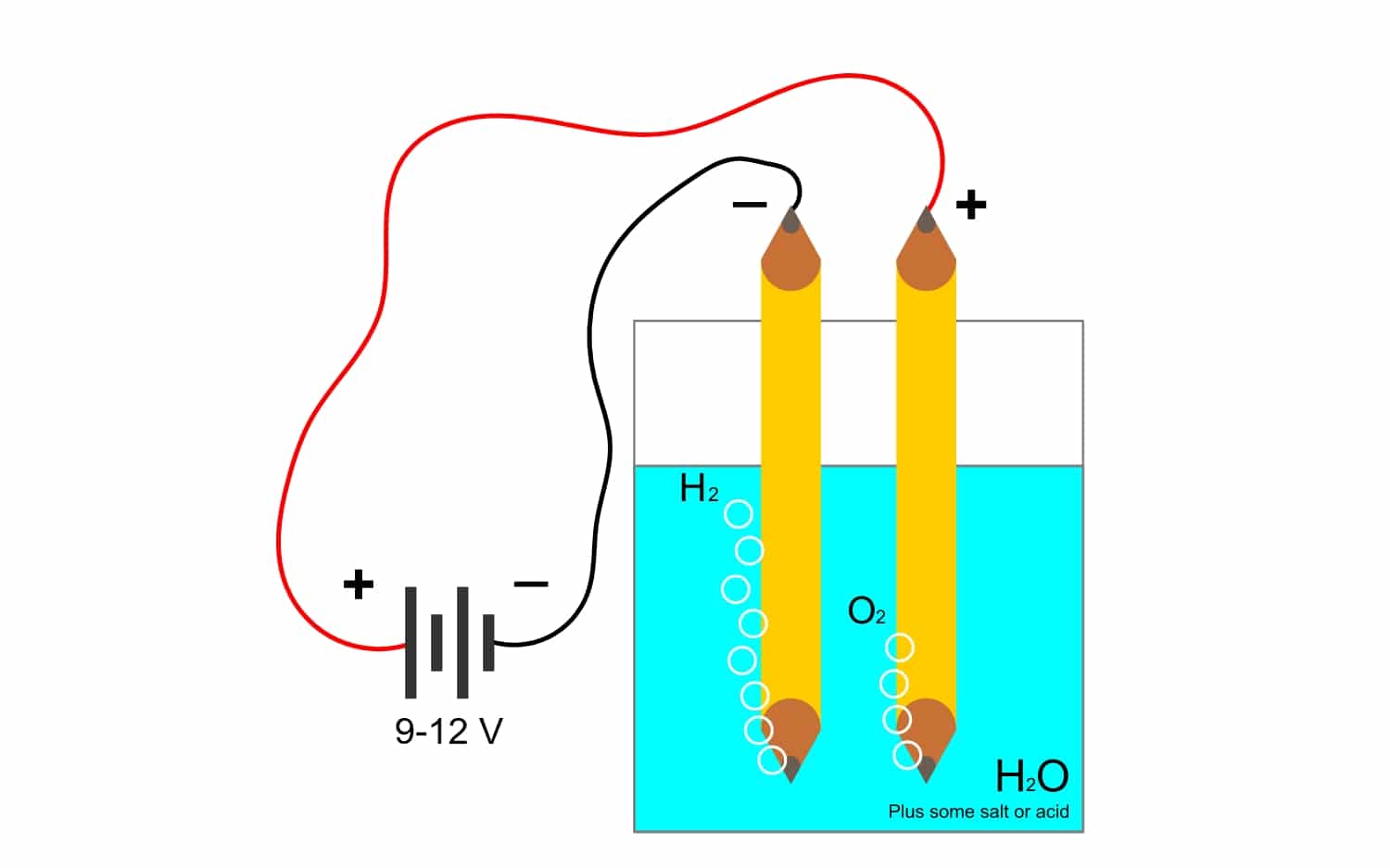
Y ya que la constante de Faraday está tan relacionada con la electrólisis, vamos a ver qué es este otro término que se emplea bastante en la industria. Gracias a este proceso se pueden separar elementos de un compuesto por medio de electricidad. Esto se hace mediante la liberación de electrones por los aniones del ánodo (oxidación) y la captura de electrones por los cationes del cátodo (reducción).
Fue descubierta accidentalmente por William Nicholson, en 1800, mientrs estudiaba el funcionamiento de las baterías químicas. En 1834, Michael Faraday desarrolló y publicó las leyes de la electrólisis.
Por ejemplo, la electrólisis del agua H2O, permite crear oxígeno e hidrógeno. Si se le aplica un corriente continua a través de unos electrodos, lo que conseguirá separar el oxígeno del hidrógeno, y poder aislar ambos gases (no pueden entrar en contacto, ya que producen una reacción explosiva muy peligrosa).