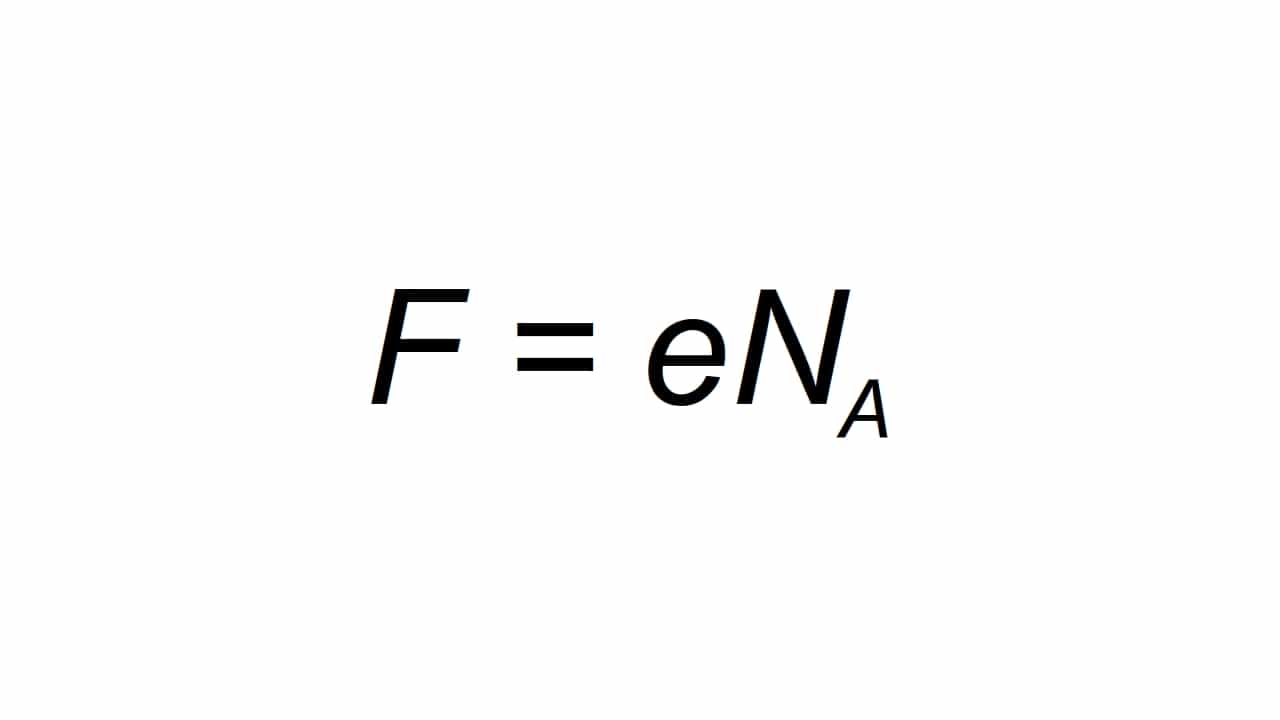Ashtu si herëve të tjera, ne kemi komentuar pyetje të tjera themelore në fushën e elektronikës dhe energjisë elektrike, të tilla si Ligji i Ohmit, dallgët Ligjet e Kirchoff, dhe madje edhe llojet e qarqeve elektrike bazë, do të ishte gjithashtu interesante të dihet se çfarë është Konstanta e Faraday, pasi mund t'ju ndihmojë të dini pak më shumë për ngarkesat.
Në këtë artikull do të kuptoni pak më mirë çfarë është lumturi konstante, për çfarë mund të aplikohet dhe si llogaritet ...
Cila është konstantja Faraday?
La Konstanta e Faraday është një konstante e përdorur gjerësisht në fushat e fizikës dhe kimisë. Përkufizohet si sasia e ngarkesës elektrike për mol të elektroneve. Emri i tij vjen nga shkencëtari britanik Michael Faraday. Kjo konstante mund të përdoret në sistemet elektrokimike për të llogaritur masën e elementeve që formohen në një elektrodë.
Mund të përfaqësohet me shkronjë F, dhe përcaktohet si ngarkesa elementare molare, duke qenë në gjendje llogarit si:
të qenë F vlera që rezulton të konstantës së Farday, e ngarkesës elementare elektrike, dhe Na është konstante e Avogadro:
- e = 1.602176634 10-19 C
- Na = 6.02214076 × 1023 mol-1
Sipas SI kjo konstante Faraday është e saktë, si konstantet e tjera, dhe vlera e saj e saktë është: 96485,3321233100184 C / molMe Siç mund ta shihni, ajo shprehet në njësinë C / mol, domethënë coulombs për mole. Dhe për të kuptuar se cilat janë këto njësi, nëse nuk e dini ende, mund të vazhdoni të lexoni dy pjesët e ardhshme ...
Çfarë është një nishan?
Un mol është një njësi që mat sasinë e substancës. Brenda SI të njësive, është një nga 7 madhësitë themelore. Në çdo substancë, qoftë një element apo një përbërje kimike, ka një seri njësish elementare që e përbëjnë atë. Një nishan do të ishte ekuivalent me 6,022 140 76 × 1023 entitetet elementare, e cila është vlera fikse numerike e konstantës së Avogadro.
Këto entitete elementare mund të jenë një atom, një molekulë, një jon, një elektron, fotone ose ndonjë lloj tjetër grimce elementare. Për shembull, me këtë ju mundeni njehso numrin e atomeve çfarë është në një gram të një substance të caktuar.
Në kimi, nishani është thelbësor, pasi lejon të bëhen shumë llogaritje për kompozimet, reaksionet kimike, etj. Për shembull, për ujin (H2O), ju keni një reagim 2 H2 + OSE2 H 2 orë2O, domethënë, se dy mole hidrogjen (H2) dhe një mol oksigjen (O2) reagojnë për të formuar dy mole ujë. Për më tepër, ato gjithashtu mund të përdoren për të shprehur përqendrimin (shih molaritetin).
Çfarë është ngarkesa elektrike?
Nga ana tjetër, nga ngarkesë elektrike Ne kemi folur tashmë në raste të tjera, është një veti e brendshme fizike e disa grimcave nënatomike që shfaqin forca tërheqëse dhe neveritëse midis tyre për shkak të fushave elektromagnetike. Ndërveprimi elektromagnetik, midis ngarkesës dhe fushës elektrike, është një nga 4 ndërveprimet themelore në fizikë, së bashku me forcën e fortë bërthamore, forcën e dobët bërthamore dhe forcën gravitacionale.
Për të matur këtë ngarkesë elektrike, Coulomb (C) ose Coulomb, dhe përcaktohet si sasia e ngarkesës që bartet në një sekondë nga një rrymë elektrike me intensitet një amper.
Aplikimet e konstantes Faraday

Nëse pyet veten se çfarë aplikim praktik Ju mund ta keni këtë konstante Faraday, e vërteta është se ju keni mjaft, disa shembuj janë:
- Lustrim / anodizim: për proceset në industrinë metalurgjike ku një metal është i mbuluar me një tjetër me elektrolizë. Për shembull, kur çeliku është i galvanizuar me një shtresë zinku për t'i dhënë atij rezistencë më të madhe ndaj korrozionit. Në këto procese, metali që do të veshet përdoret si anodë dhe elektroliti është një kripë e tretshme e materialit të anodës.
- Pastrimi i metaleve: mund të aplikohet edhe në formulat e përdorura për rafinimin e metaleve si bakri, zinku, kallaji, etj. Gjithashtu nga procedurat e elektrolizës.
- Prodhim kimik: për të prodhuar komponime kimike kjo konstante përdoret gjithashtu zakonisht.
- Analiza kimike: me elektrolizë mund të përcaktohej edhe përbërja kimike.
- Prodhimi i gazit: gazrat si oksigjeni ose hidrogjeni që merren nga uji me elektrolizë gjithashtu e përdorin këtë konstante për llogaritjet.
- Mjekësia dhe estetikaElektroliza gjithashtu mund të përdoret për të stimuluar nerva të caktuara ose për të trajtuar probleme të caktuara, përveç heqjes së qimeve të padëshiruara. Pa konstanten, një mori mjetesh të këtij lloji nuk do të mund të ishin zhvilluar.
- Shtyp: Për printerët, proceset e elektrolizës përdoren gjithashtu për elementë të caktuar.
- Kondensatorët elektrolitikë: një komponent i njohur elektronik i përbërë nga një film i hollë i oksidit të aluminit dhe një anodë alumini midis elektrodave. Elektroliti është një përzierje e acidit borik, glicerinës dhe hidroksidit të amonit. Dhe kështu arrihen ato kapacitete të mëdha ...
Çfarë është elektroliza?
Dhe meqenëse konstanta Faraday është aq e lidhur ngushtë me elektrolizaLe të shohim se çfarë është ky term tjetër që përdoret shumë në industri. Falë këtij procesi, elementët e një kompleksi mund të ndahen me anë të energjisë elektrike. Kjo bëhet me lëshimin e elektroneve nga anionet e anodës (oksidimi) dhe kapjen e elektroneve nga kationet katodike (reduktimi).
U zbulua rastësisht nga William Nicholson, në 1800, ndërsa studionte funksionimin e baterive kimike. Në 1834, Michael faraday zhvilloi dhe publikoi ligjet e elektrolizës.
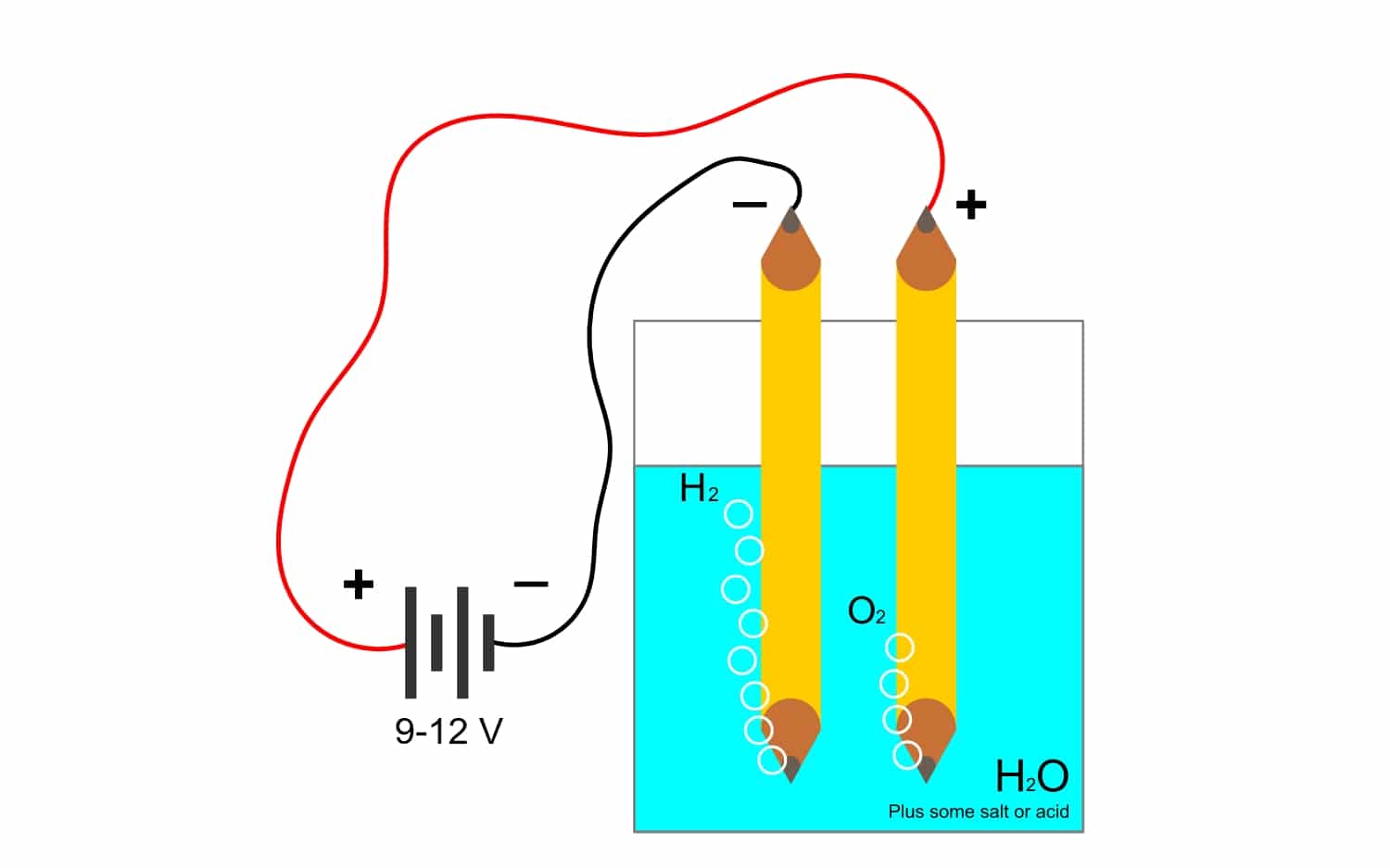
Për shembull, elektroliza e ujë H2O, lejon krijimin e oksigjenit dhe hidrogjenit. Nëse një rrymë e drejtpërdrejtë aplikohet përmes elektrodave, të cilat do të ndajnë oksigjenin nga hidrogjeni dhe do të jenë në gjendje të izolojnë të dy gazrat (ato nuk mund të vijnë në kontakt, pasi ato prodhojnë një reagim shpërthyes shumë të rrezikshëm).